Apidra za zdravljenje sladkorne bolezni
Blagovna znamka: Apidra
Generično ime: Insulin Glulisine
Apidra (insulin glulisine) je umetni izdelek, ki je skoraj enak človeškemu insulinu. Uporablja se za zdravljenje diabetesa mellitusa. Uporaba, odmerjanje, stranski učinki.
Vsebina:
Indikacije in uporaba
Odmerjanje in uporaba
Kontraindikacije
Opozorila in previdnostni ukrepi
Neželeni učinki
Interakcije z zdravili
Uporaba v posebnih populacijah
Preveliko odmerjanje
Opis
Klinična farmakologija
Neklinična toksikologija
Klinične študije
Kako dobavljeno
Apidra, insulin glusin, podatki o bolniku (v navadni angleščini)
Indikacije
Apidra je hitro delujoči humani analog insulina, ki je indiciran za izboljšanje nadzora glikemije pri odraslih in otrocih z diabetesom mellitusom.
vrh
Odmerjanje in uporaba
Upoštevanje odmerjanja
APIDRA je rekombinantni analog insulina, ki je enakovreden humanemu insulinu (tj. Ena enota APIDRA ima enak učinek zniževanja glukoze kot ena enota običajnega humanega insulina), če ga dajemo intravensko. Če ga dajemo subkutano, ima APIDRA hitreje začetek delovanja in krajše trajanje delovanja kot običajni humani insulin.
Odmerjanje zdravila APIDRA mora biti individualizirano. Spremljanje glukoze v krvi je nujno pri vseh bolnikih, ki prejemajo zdravljenje z insulinom.
Skupna dnevna potreba po insulinu se lahko razlikuje in je običajno med 0,5 do 1 enoto / kg / dan. Potrebe po insulinu se lahko spremenijo med stresom, večjimi boleznimi ali s spremembami telesne vadbe, vzorcev obroka ali sočasno jemljenih zdravil.
Subkutana uporaba
Zdravilo APIDRA je treba dajati v 15 minutah pred obrokom ali v 20 minutah po začetku obroka.
Zdravilo APIDRA, ki ga dajemo s subkutano injekcijo, se običajno uporablja v shemah z vmesnim ali dolgo delujočim insulinom.
Zdravilo APIDRA je treba dajati s subkutano injekcijo v trebušno steno, stegno ali nadlaket. Mesta injiciranja je treba zasukati znotraj iste regije (trebuh, stegno ali nadlaket) od ene injekcije do druge, da zmanjšate tveganje za lipodistrofijo [glejte NEŽELENI REAKCI].
Neprekinjena podkožna infuzija (inzulinska črpalka)
Zdravilo APIDRA se lahko daje s kontinuirano podkožno infuzijo v trebušni steni. Ne uporabljajte razredčenih ali mešanih insulinov v zunanjih insulinskih črpalkah. Mesto infuzije je treba zasukati znotraj iste regije, da se zmanjša tveganje za lipodistrofijo [Glej NEŽELENI REAKCI]. Začetno programiranje zunanje infuzijske črpalke insulina mora temeljiti na skupnem dnevnem odmerku insulina v prejšnjem režimu.
V kliničnih preskušanjih APIDRA, ki jih je opravil sanofi-aventis, proizvajalec APIDRA, so bile uporabljene naslednje črpalke inzulina:
- Disetronic® H-Tron® plus V100 in D-Tron® z Disetronic katetri (Rapid ™, Rapid C ™, Rapid D ™ in Tender ™)
- MiniMed® Modeli 506, 507, 507c in 508 s MiniMed katetri (Sof set Ultimate QR ™ in Quick-set ™).
Pred uporabo druge insulinske črpalke z APIDRA preberite nalepko črpalke in se prepričajte, da je bila črpalka ovrednotena z APIDRA.
Zdravniki in pacienti morajo natančno oceniti podatke o uporabi črpalk v navodilih za predpisovanje APIDRA, navodilih za bolnike in priročniku proizvajalca črpalke. Za čas uporabe, pogostnost spreminjanja infuzijskih setov ali drugo je treba upoštevati informacije, specifične za APIDRA podrobnosti, značilne za uporabo APIDRA, ker se lahko podatki, specifični za APIDRA, razlikujejo od splošnih navodil za črpanje navodila.
Na podlagi raziskav in vitro, ki so pokazale izgubo konzervansa, metakrezola in razgradnjo insulina, je treba APIDRA v rezervoarju spremeniti vsaj vsakih 48 ur. APIDRA v klinični uporabi ne sme biti izpostavljena temperaturam (37 ° C) nad 98,6 ° F. [Glej OPOZORILA IN VARNOSTNI UKREPI in KAKO DOSTAVA / Skladiščenje in ravnanje].
Intravensko dajanje
Zdravilo APIDRA se lahko daje intravensko pod zdravniškim nadzorom za nadzor glikemije s natančnim nadzorom glukoze v krvi in kalija v serumu, da se prepreči hipoglikemija in hipokalemija. Za intravensko uporabo je treba APIDRA uporabljati v koncentracijah 0,05 enot / ml do 1 enote / ml insulina glulisina v infuzijskih sistemih z uporabo vrečic iz polivinilklorida (PVC). Za APIDRA se je izkazalo, da je stabilen le v običajni fiziološki raztopini (0,9% natrijevega klorida). Parenteralno uporabo zdravil je treba pred uporabo vizualno pregledati, ali vsebuje delce in razbarvanje, kadar to dovoljuje raztopina in posoda. Ne dajajte zmesi insulina intravensko.
Odmerne oblike in jakosti
Apidra 100 enot na ml (U-100) je na voljo kot:
- 10 ml viale
- 3 ml kartuše za uporabo v OptiClik® Naprava za dostavo insulina
- 3 ml napolnjeni injekcijski peresnik SoloStar
vrh
Kontraindikacije
Apidra je kontraindicirana:
- med epizodami hipoglikemije
- pri bolnikih, ki so preobčutljivi za zdravilo Apidra ali katero koli njegovo pomožno snov
Če se uporablja pri bolnikih z znano preobčutljivostjo za Apidro ali njegove pomožne snovi, lahko bolniki razvijejo lokalizirane ali splošne preobčutljivostne reakcije [Glej Neželeni učinki].
vrh
Opozorila in previdnostni ukrepi
Prilagajanje odmerka in spremljanje
Spremljanje glukoze je nujno pri bolnikih, ki prejemajo zdravljenje z insulinom. Spremembe režima insulina je treba izvajati previdno in le pod zdravniškim nadzorom. Spremembe jakosti insulina, proizvajalca, vrste ali načina dajanja lahko povzročijo potrebo po spremembi odmerka insulina. Mogoče bo treba prilagoditi sočasno zdravljenje z antidiabetiki.
Kot pri vseh zdravilih z insulinom se lahko časovni potek delovanja zdravila Apidra pri posameznih posameznikih ali v različnih obdobjih v tem času razlikuje isti posameznik in je odvisen od mnogih stanj, vključno z mestom injiciranja, lokalno oskrbo s krvjo ali lokalno temperatura. Bolnikom, ki spremenijo raven telesne aktivnosti ali načrt obrokov, bo morda treba prilagoditi odmerjanje insulina.
Hipoglikemija
Hipoglikemija je najpogostejši neželeni učinek zdravljenja z insulinom, vključno z zdravilom Apidra. S poostrenim nadzorom glikemije se poveča tveganje za hipoglikemijo. Bolnike je treba izobraževati za prepoznavanje in obvladovanje hipoglikemije. Huda hipoglikemija lahko privede do nezavesti in / ali krčev in lahko povzroči začasno ali trajno okvaro možganske funkcije ali smrt. Huda hipoglikemija, ki zahteva pomoč druge osebe in / ali parenteralna infuzija glukoze oz V kliničnih preskušanjih z insulinom, vključno s preskušanji z glukagonom, so opazili uporabo glukagona Apidra.
Čas hipoglikemije običajno odraža profil časovnega delovanja danih insulinskih formulacij. Drugi dejavniki, kot so spremembe vnosa hrane (npr. Količina hrane ali čas obrokov), mesto injiciranja, vadba in sočasna zdravila lahko prav tako spremenijo tveganje za hipoglikemijo [glejte Interakcije z zdravili].
Kot pri vseh insulinih, bodite previdni pri bolnikih, ki ne poznajo hipoglikemije, in pri bolnikih, ki so morda nagnjeni k hipoglikemiji (npr. pri pediatrični populaciji in bolnikih, ki postijo ali imajo napačno hrano vnos). Bolnikova sposobnost koncentracije in reakcije je lahko oslabljena kot posledica hipoglikemije. To lahko predstavlja tveganje v situacijah, ko so te sposobnosti še posebej pomembne, na primer vožnja ali upravljanje drugih strojev.
Hitro spreminjanje ravni glukoze v serumu lahko povzroči simptome, podobne hipoglikemiji, pri osebah s sladkorno boleznijo, ne glede na vrednost glukoze. Zgodnji opozorilni simptomi hipoglikemije so lahko pod določenimi pogoji različni ali manj izraziti, kot so dolgoletna diabetes, bolezen diabetičnih živcev, uporaba zdravil, kot so zaviralci beta [Glej Interakcije z zdravili], ali intenzivnejši nadzor sladkorne bolezni. Te situacije lahko povzročijo hudo hipoglikemijo (in po možnosti tudi izgubo zavesti), preden se bolnik zaveda hipoglikemije.
Intravensko dani insulin ima hitrejši začetek delovanja kot subkutano inzulin, ki zahteva natančnejše spremljanje hipoglikemije.
Preobčutljivost in alergijske reakcije
Pri izdelkih z insulinom, vključno z zdravilom Apidra, se lahko pojavi resna, življenjsko nevarna generalizirana alergija, vključno z anafilaksijo [glejte Neželeni učinki].
Hipokalemija
Vsi izdelki z insulinom, vključno z Apidro, povzročajo premik kalija iz zunajceličnega v medcelični prostor, kar lahko vodi v hipokalemijo. Nezdravljena hipokalemija lahko povzroči respiratorno paralizo, ventrikularno aritmijo in smrt. Bodite previdni pri bolnikih, pri katerih obstaja nevarnost hipokalemije (npr. Pri bolnikih, ki uporabljajo zdravila za zniževanje kalija, pri bolnikih, ki jemljejo zdravila, občutljiva na koncentracijo kalija v serumu). Kadar se zdravilo Apidra daje intravensko, pogosto spremljajte glukozo in kalij.
Okvara ledvic ali jeter
Pri bolnikih z ledvično ali jetrno okvaro bo morda potreben pogost nadzor glukoze in zmanjšanje odmerka insulina [Glej Klinična farmakologija].
Mešanje insulinov
Apidre za subkutano injiciranje ne smemo mešati z inzulinskimi pripravki, ki niso inzulin NPH. Če zmešamo Apidra z insulinom NPH, je treba zdravilo Apidra najprej potegniti v brizgo. Injekcija se mora pojaviti takoj po mešanju.
Zdravila Apidra ne mešajte z drugimi insulini za intravensko aplikacijo ali za uporabo v neprekinjeni podkožni infuzijski črpalki.
Zdravila Apidra za intravensko uporabo ne smemo razredčiti z raztopinami, ki niso 0,9% natrijevega klorida (običajna fiziološka raztopina). Učinkovitost in varnost mešanja zdravila Apidra z razredčili ali drugimi insulini za uporabo v zunanjih podkožnih črpalkah za infundiranje nista bili ugotovljeni.
Podkožne črpalke za infundiranje insulina
Pri uporabi v zunanji inzulinski črpalki za podkožno infuzijo zdravila Apidra ne smete razredčiti ali mešati z drugim insulinom. Apidro v rezervoarju je treba menjati vsaj vsakih 48 ur. Apidre ne smemo izpostavljati temperaturam, večjim od 37 ° C.
Nepravilno delovanje insulinske črpalke ali infuzijskega kompleta ali razgradnja insulina lahko hitro privede do hiperglikemije in ketoze. Potrebno je hitro prepoznati in odpraviti vzrok hiperglikemije ali ketoze. Morda bodo potrebne vmesne subkutane injekcije zdravila Apidra. Bolniki, ki uporabljajo kontinuirano terapijo s subkutano infuzijo z insulinom, morajo biti usposobljeni za aplikacijo insulina z injekcijo in na voljo nadomestno zdravljenje z insulinom v primeru odpovedi črpalke. [Glej Odmerjanje in uporaba, Kako dobava / skladiščenje in ravnanje].
Intravensko dajanje
Pri intravenski uporabi zdravila Apidra je treba natančno nadzorovati raven glukoze in kalija, da se prepreči potencialno usodna hipoglikemija in hipokalemija.
Zdravila Apidra ne mešajte z drugimi insulini za intravensko aplikacijo. Apidra se lahko razredči le v običajni fiziološki raztopini.
Interakcije z drogami
Nekatera zdravila lahko spremenijo potrebo po insulinu in tveganje za hipoglikemijo ali hiperglikemijo [Glej Interakcije z zdravili].
vrh
Neželeni učinki
Naslednji neželeni učinki so obravnavani drugje:
- Hipoglikemija [Glej Opozorila in previdnostni ukrepi]
- Hipokalemija [Glej Opozorila in previdnostni ukrepi]
Izkušnje s kliničnim preskušanjem
Ker se klinična preskušanja izvajajo v zelo različnih izvedbah, stopnje neželenih učinkov, o katerih so poročali v enem kliničnem preskušanju, morda ne bodo zlahka primerjati s stopnjami, o katerih so poročali v drugem kliničnem preskušanju, in morda ne odraža stopnje, ki so jo dejansko opazili v kliničnem preskušanju vadite.
Pogostost neželenih učinkov med kliničnimi preskušanji zdravila Apidra pri bolnikih z diabetesom mellitusom tipa 1 in diabetesom mellitusom tipa 2 je navedena v spodnjih tabelah.
Tabela 1: Zdravilni neželeni učinki v združenih študijah pri odraslih s sladkorno boleznijo tipa 1 (neželeni učinki s pogostostjo ¥ ¥ 5%)
| APIDRA,% (n = 950) |
Vsi primerjalnikia, % (n = 641) |
|
| Nazofaringitis | 10.6 | 12.9 |
| Hipoglikemijab | 6.8 | 6.7 |
| Okužba zgornjih dihal | 6.6 | 5.6 |
| Gripa | 4.0 | 5.0 |
|
a Insulin lispro, navadni humani insulin, inzulin aspart b Le huda simptomatska hipoglikemija |
Tabela 2: Neželeni učinki zdravljenja v skupnih študijah pri odraslih s sladkorno boleznijo tipa 2 (neželeni učinki s pogostostjo â ¥ 5%)
| APIDRA,% (n = 883) |
Redni humani inzulin,% (n = 883) |
|
| Okužba zgornjih dihal | 10.5 | 7.7 |
| Nazofaringitis | 7.6 | 8.2 |
| Periferni edem | 7.5 | 7.8 |
| Gripa | 6.2 | 4.2 |
| Artralgija | 5.9 | 6.3 |
| Hipertenzija | 3.9 | 5. |
- Pediatrija
Tabela 3 povzema neželene učinke, ki so se pojavili s pogostostjo večjo od 5% v klinični študiji pri otrocih in mladostnikih s sladkorno boleznijo tipa 1, zdravljenih z APIDRA (n = 277) ali insulinom lispro (n = 295).
Tabela 3: Zdravljenje - neželeni učinki pri otrocih in mladostnikih s sladkorno boleznijo tipa 1 (neželeni učinki s pogostostjo 5%)
| APIDRA,% (n = 277) |
Lispro,% (n = 295) |
|
| Nazofaringitis | 9.0 | 9.5 |
| Okužba zgornjih dihal | 8.3 | 10.8 |
| Glavobol | 6.9 | 11.2 |
| Hipoglikemični napad | 6.1 | 4.7 |
- Huda simptomatska hipoglikemija
Hipoglikemija je najpogostejši neželeni učinek pri bolnikih, ki uporabljajo insulin, vključno z zdravilom Apidra [Glej Opozorila in previdnostni ukrepi]. Stopnje in pojavnost hude simptomatske hipoglikemije, opredeljene kot hipoglikemija, ki zahteva posredovanje tretje osebe, sta bila primerljiva za vse sheme zdravljenja (glejte tabelo 4). V kliničnem preskušanju faze 3 so imeli večjo pojavnost otroci in mladostniki s sladkorno boleznijo tipa 1 hude simptomatske hipoglikemije v obeh skupinah zdravljenja v primerjavi z odraslimi s tipom 1 diabetes. (glej tabelo 4) [Glej Klinične študije].
Tabela 4: Huda simptomatska hipoglikemija *
| Diabetes tipa 1 Odrasli 12 tednov z insulinom glargin |
Diabetes tipa 1 odrasli 26 tednov z insulinom glargin |
Diabetes tipa 2 Odrasli 26 tednov s človeškim insulinom NPH |
Diabetes tipa 1 26 tednov |
||||||
|---|---|---|---|---|---|---|---|---|---|
| Apidra Pred obrokom |
Apidra Po obroku |
Redni človeški inzulin | Apidra | Insulin Lispro | Apidra | Redni človeški inzulin | Apidra | Insulin Lispr | |
| * Huda simptomatska hipoglikemija, opredeljena kot hipoglikemični dogodek, za katerega je potrebna pomoč druge osebe, ki izpolnjuje eno od naslednjih meril: dogodek je bil povezan s krvjo v glukozi v krvi, manjšo od 36 mg / dl, ali pa je bil povezan s takojšnjim okrevanjem po peroralni uporabi ogljikovih hidratov, intravenski uporabi glukoze ali glukagona. | |||||||||
| Dogodki na mesec na pacienta | 0.05 | 0.05 | 0.13 | 0.02 | 0.02 | 0.00 | 0.00 | 0.09 | 0.08 |
| Odstotek bolnikov (n / skupno N) | 8.4% (24/286) | 8.4% (25/296) | 10.1% (28/278) | 4.8% (16/339) |
4.0% (13/333) |
1.4% (6/416) |
1.2% (5/420) |
16.2% (45/277) |
19.3% (57/295) |
- Začetek inzulina in intenziviranje kontrole glukoze
Intenzifikacija ali hitro izboljšanje nadzora glukoze je povezano s prehodnim, reverzibilnim motnja oftalmološke refrakcije, poslabšanje diabetične retinopatije in akutna boleča periferna nevropatija. Vendar dolgotrajna kontrola glikemije zmanjšuje tveganje za diabetično retinopatijo in nevropatijo.
- Lipodistrofija
Dolgotrajna uporaba insulina, vključno z Apidro, lahko povzroči lipodistrofijo na mestu ponavljajočih se injekcij ali infundiranja insulina. Lipodistrofija vključuje lipohipertrofijo (zgostitev maščobnega tkiva) in lipoatrofijo (tanjšanje maščobnega tkiva) in lahko vpliva na absorpcijo insulina. Zavrtite mesta injiciranja ali infuzije na istem območju, da zmanjšate tveganje za lipodistrofijo. [Glej Odmerjanje in uporaba].
- Povečanje telesne mase
Povečanje telesne mase se lahko pojavi z zdravljenjem z insulinom, vključno z zdravilom Apidra, in se pripisuje anaboličnim učinkom insulina in zmanjšanju glukozurije.
- Periferni edem
Inzulin, vključno z Apidro, lahko povzroči zadrževanje natrija in edeme, zlasti če se predhodno slabši metabolični nadzor izboljša z intenzivnejšim zdravljenjem z insulinom.
- Neželeni učinki s kontinuirano subkutano infuzijo insulina (CSII)
V 12-tedenski randomizirani študiji pri bolnikih s sladkorno boleznijo tipa 1 (n = 59) stopnja katetra okluzije in reakcije na mestu infuzije so bile podobne pri bolnikih, zdravljenih z zdravilom Apidra in z insulinom aspart (Tabela 5).
Tabela 5: Okluzije katetra in reakcije na mestu infuzije.
| Apidra (n = 29) |
inzulin aspart (n = 30) |
|
|---|---|---|
| Okluzije katetra / mesec | 0.08 | 0.15 |
| Reakcije na mestu infuzije | 10.3% (3/29) | 13.3% (4/30) |
- Alergijske reakcije
Lokalna alergija
Kot pri vsaki terapiji z insulinom, lahko tudi pri bolnikih, ki jemljejo zdravilo Apidra, na mestu injiciranja pojavijo pordelost, otekanje ali srbenje. Te manjše reakcije običajno izzvenijo v nekaj dneh do nekaj tednih, v nekaterih primerih pa lahko zahtevajo tudi ukinitev zdravila Apidra. V nekaterih primerih so te reakcije lahko povezane z dejavniki, ki niso inzulin, kot so dražilna sredstva za čiščenje kože ali slaba tehnika injiciranja.
Sistemska alergija
Pri katerem koli insulinu, vključno z zdravilom Apidra, se lahko pojavi resna, življenjsko nevarna generalizirana alergija, vključno z anafilaksijo. Splošna alergija na inzulin lahko povzroči izpuščaje na celotnem telesu (vključno s srbenjem), dispnejo, piskajočim sopenjem, hipotenzijo, tahikardijo ali diaforezo.
V nadzorovanih kliničnih preskušanjih, ki so trajale 12 mesecev, so o možnih sistemskih alergijskih reakcijah poročali pri 79 bolnikih 1833 bolnikov (4,3%), ki so prejeli zdravilo Apidra, in 58 od 1524 bolnikov (3,8%), ki so primerjali kratkotrajno delovanje insulini. Med temi preskušanji je bilo zdravljenje z zdravilom Apidra trajno prekinjeno pri 1 od 1833 bolnikov zaradi možne sistemske alergijske reakcije.
Pri uporabi metakresola, ki je pomožna snov zdravila Apidra, so poročali o lokaliziranih reakcijah in splošni mialgiji.
Proizvodnja protiteles
V študiji pri bolnikih s sladkorno boleznijo tipa 1 (n = 333) so koncentracije insulinskih protiteles, ki reagirajo tako s človeškim insulinom kot insulinom glulisin (navzkrižno reaktivno inzulinsko protitelo) je v prvih šestih mesecih študije pri bolnikih, zdravljenih z Apidra. V naslednjih 6 mesecih študije so opazili zmanjšanje koncentracije protiteles. V študiji pri bolnikih s sladkorno boleznijo tipa 2 (n = 411) je bilo podobno povečanje koncentracije navzkrižno reaktivnih protiteles opazili pri bolnikih, ki so se zdravili z zdravilom Apidra, in pri bolnikih, ki so v prvih 9 mesecih prejemali humani insulin študij. Nato se je koncentracija protiteles pri bolnikih z zdravilom Apidra zmanjšala in ostala stabilna pri bolnikih z insulinom. Med navzkrižno reaktivno koncentracijo protitelesa inzulina in spremembami HbA1c, odmerkom insulina ali pogostostjo hipoglikemije ni bilo povezave. Klinični pomen teh protiteles ni znan.
Apidra ni pokazala pomembnega odziva na protitelesa v študiji otrok in mladostnikov s sladkorno boleznijo tipa 1.
Postmarketing izkušnja
Naslednji neželeni učinki so bili ugotovljeni med uporabo zdravila Apidra po odobritvi zdravila.
Ker se o teh reakcijah poroča prostovoljno iz populacije negotove velikosti, ni vedno mogoče zanesljivo oceniti njihovo pogostost ali vzpostaviti vzročno zvezo z drogo izpostavljenost.
Poročali so o napakah v zdravljenju, pri katerih so namesto zdravila Apidra po naključju dajali druge insuline, zlasti dolgo delujoče.
vrh
Interakcije z zdravili
Številna zdravila vplivajo na presnovo glukoze in lahko zahtevajo prilagajanje odmerka insulina in zlasti natančno spremljanje.
Zdravila, ki lahko povečajo učinek insulinov na zniževanje glukoze v krvi, vključno z zdravilom Apidra, in zato povečajo tveganje za hipoglikemijo, vključujejo peroralna antidiabetična zdravila, pramlintid, zaviralci ACE, disopiramid, fibrati, fluoksetin, zaviralci monoamin oksidaze, propoksifen, pentoksifilin, salicilati, analogi somatostatina in sulfonamid antibiotiki.
Zdravila, ki lahko zmanjšajo učinek zdravila Apidra na zniževanje glukoze v krvi, vključujejo kortikosteroide, niacin, danazol, diuretike, simpatomimetična zdravila (npr. Epinefrin, albuterol, terbutalin), glukagon, izoniazid, fenotiazinski derivati, somatropin, ščitnični hormoni, estrogeni, progestogeni (npr. pri peroralnih kontraceptivih), zaviralci proteaze in atipični antipsihotiki.
Zaviralci beta, klonidin, litijeve soli in alkohol lahko povečajo ali zmanjšajo učinek insulina na znižanje glukoze v krvi.
Pentamidin lahko povzroči hipoglikemijo, ki ji lahko včasih sledi hiperglikemija.
Znaki hipoglikemije so lahko zmanjšani ali odsotni pri bolnikih, ki jemljejo antirenergična zdravila, kot so zaviralci beta, klonidin, gvanetidin in rezerpin.
vrh
Uporaba v posebnih populacijah
Nosečnost
Nosečnost Kategorija C: Raziskave na razmnoževanju in teratologiji so bile izvedene z insulinom glulisin pri podganah in kuncih, ki so kot primerjalnik uporabljali navadni humani insulin. Inzulinski glulisin so ženskam podgane dajale med nosečnostjo v subkutanih odmerkih do 10 enot / kg enkrat na dan (odmerek povzroči izpostavljenost 2-krat večji od povprečnega odmerka pri ljudeh glede na površino telesne površine) in ni imela izrazitih toksičnih učinkov na zarodek-plod razvoj.
Inzulinski glulisin so ženski kunci dajali med nosečnostjo v subkutanih odmerkih do 1,5 Enote / kg / dan (odmerek, zaradi katerega je izpostavljenost 0,5-krat večja od povprečnega odmerka za človeka, odvisno od telesne površine primerjava). Neželeni učinki na razvoj zarodka-ploda so bili opaženi le pri odmerjanju toksičnih odmerkov za mater, ki povzročajo hipoglikemijo. Opazili so povečano pojavnost postimplantacijskih izgub in skeletnih napak pri ravni odmerka 1,5 enote / kg enkrat na dan (odmerek zaradi česar je bila izpostavljenost 0,5-krat večja od povprečnega odmerka za človeka (glede na površino telesne površine), ki je povzročila tudi smrtnost pri jezovi. Pri naslednji naslednji ravni odmerka 0,5 enot / kg enkrat na dan so opazili rahlo povečano pojavnost izgub po implantaciji (odmerek je povzročil izpostavljenost 0,2 kratnik povprečnega odmerka pri ljudeh na podlagi primerjave telesne površine), ki je bil povezan tudi s hudo hipoglikemijo, vendar pri tem ni bilo okvar odmerek. Pri odmerkih 0,25 enot / kg enkrat na dan niso opazili učinkov (odmerek je povzročil izpostavljenost 0,1-krat večjo od povprečnega odmerka pri ljudeh na podlagi primerjave telesne površine). Učinki insulina glulisina se niso razlikovali od tistih, ki so jih opazili pri subkutanem navadnem humanem insulinu v enakih odmerkih in so jih pripisali sekundarnim učinkom materine hipoglikemije.
Kliničnih študij o uporabi zdravila Apidra pri nosečnicah ni. Ker študije razmnoževanja na živalih ne napovedujejo vedno človeškega odziva, je treba to zdravilo med nosečnostjo uporabljati le, če potencialna korist upravičuje potencialno tveganje za plod. Za bolnike s sladkorno boleznijo ali anamnezo gestacijske sladkorne bolezni je pomembno, da ohranijo dobro presnovo pred spočetjem in v celotni nosečnosti. Potrebe po insulinu se lahko med prvim trimesečjem zmanjšajo, običajno se v drugem in tretjem trimesečju povečajo in po porodu hitro upadejo. Skrbno spremljanje nadzora glukoze je pri teh bolnikih nujno.
Doječe matere
Ni znano, ali se glulin iz insulina izloča v materino mleko. Ker se v materino mleko izloča veliko zdravil, je pri zdravljenju doječe ženske potrebna previdnost. Uporaba zdravila Apidra je združljiva z dojenjem, vendar lahko ženske z diabetesom, ki dojijo, morda zahtevajo prilagoditev odmerka insulina.
Pediatrična uporaba
Varnost in učinkovitost subkutanih injekcij zdravila Apidra sta bili ugotovljeni pri otrocih (starih od 4 do 17 let) s sladkorno boleznijo tipa 1 [glej Klinične študije]. Zdravila Apidra niso preučevali pri otrocih s sladkorno boleznijo tipa 1, mlajšimi od 4 let, in pri pediatričnih bolnikih s sladkorno boleznijo tipa 2.
Kot pri odraslih je treba tudi pri pediatričnih bolnikih odmerjati zdravilo Apidra na podlagi presnovnih potreb in pogostega spremljanja glukoze v krvi.
Geriatrična uporaba
V kliničnih preskušanjih (n = 2408) so zdravilo Apidra dajali 147 bolnikom, starim 65 let, in 27 bolnikom, starim 75 let. Večina te majhne podskupine starejših bolnikov je imela sladkorno bolezen tipa 2. Spremembe vrednosti HbA1c in frekvenc hipoglikemije se glede na starost niso razlikovale. Kljub temu je potrebna previdnost pri uporabi zdravila Apidra geriatričnim bolnikom.
vrh
Preveliko odmerjanje
Prevelik inzulin lahko povzroči hipoglikemijo in še posebej, če dajemo intravensko, hipokalemijo. Blage epizode hipoglikemije običajno zdravimo s peroralno glukozo. Morda bodo potrebne prilagoditve odmerjanja drog, vzorcev obrokov ali vadbe. Težje epizode hipoglikemije s komo, epileptičnimi napadi ali nevrološkimi okvarami se lahko zdravijo z intramuskularno / subkutano glukagonom ali koncentrirano intravensko glukozo. Trajni vnos ogljikovih hidratov in opazovanje bodo morda potrebni, ker se lahko hipoglikemija po navideznem kliničnem okrevanju ponovi. Hipokalemijo je treba ustrezno odpraviti.
Opis
Apidra® (injiciranje insulina glulisin [rDNA izvora]) je hitro delujoči analog humanega insulina, ki se uporablja za zniževanje glukoze v krvi. Insulinski glulisin nastaja s tehnologijo rekombinantne DNA z uporabo nepatogenega laboratorijskega seva Escherichia coli (K12). Insulin glulisina se od humanega insulina razlikuje po tem, da je aminokislina asparagin v položaju B3 zamenjana z lizinom in lizin v položaju B29 zamenja glutamična kislina. Kemično je insulin glulisin 3B-lizin-29B-glutaminska kislina-človeški inzulin, ima empirično formulo C258H384N64O78S6 in molekulsko maso 5823 ter ima naslednjo strukturno formulo:
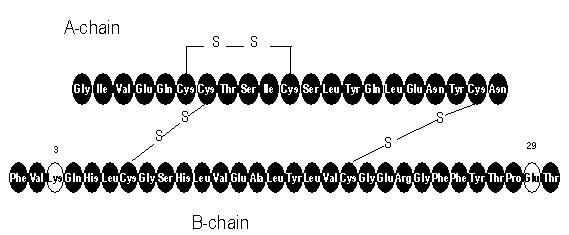
Apidra je sterilna, vodna, bistra in brezbarvna raztopina. Vsak mililiter zdravila Apidra vsebuje 100 enot (3,49 mg) insulina glulisin, 3,15 mg metakrezola, 6 mg trometamina, 5 mg natrijevega klorida, 0,01 mg polisorbata 20 in vode za injiciranje. PH apidre je približno 7,3. PH prilagodimo z dodatkom vodnih raztopin klorovodikove kisline in / ali natrijevega hidroksida.
vrh
Klinična farmakologija
Mehanizem delovanja
Uravnavanje presnove glukoze je glavna aktivnost insulinov in insulinskih analogov, vključno z insulinom glulisin. Insulini znižujejo glukozo v krvi s spodbujanjem perifernega vnosa glukoze s skeletnimi mišicami in maščobami in z zaviranjem proizvodnje glukoze v jetrih. Insulini zavirajo lipolizo in proteolizo ter pospešujejo sintezo beljakovin.
Dejavnosti Apidre in običajnega humanega insulina za zniževanje glukoze so enakovredne, kadar jih dajemo intravensko. Po subkutanem dajanju je učinek zdravila Apidra hitrejši na začetku in krajšega trajanja v primerjavi z običajnim človeškim insulinom. [Glejte Farmakodinamika].
Farmakodinamika
Študije na zdravih prostovoljcih in bolnikih s sladkorno boleznijo so pokazale, da ima zdravilo Apidra hitrejše začetek delovanja in krajše trajanje aktivnosti kot običajni humani insulin, če ga dajemo podkožno.
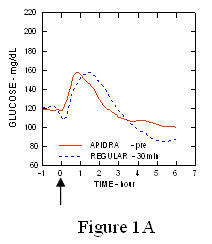
V študiji pri bolnikih s sladkorno boleznijo tipa 1 (n = 20) so bili profili za zniževanje glukoze zdravila Apidra in običajni humani insulin so v različnih obdobjih ocenjevali glede na standardni obrok v odmerku 0,15 Enote / kg (Slika 1.)
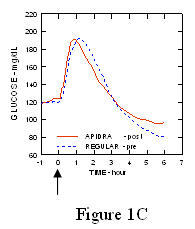
Največja ekskurzija glukoze v krvi (Î ”GLUmax; osnovna odšteta koncentracija glukoze) za zdravilo Apidra, ki ga injiciramo 2 minuti pred obrokom, je bilo 65 mg / dl v primerjavi s 64 mg / dl pri običajnem človeku injiciranje inzulina 30 minut pred obrokom (glej sliko 1A), in 84 mg / dl za običajni humani insulin, ki ga injiciramo 2 minuti pred obrokom (glejte sliko 1B). Najvišji izlet glukoze v krvi za zdravilo Apidra, ki so ga injicirali 15 minut po začetku obroka, je bil 85 mg / dL v primerjavi z 84 mg / dL pri običajnem humanem insulinu, ki ga injiciramo 2 minuti pred obrokom (glejte sliko 1C).
Slika 1. Serijska povprečna glukoza v krvi se je zbrala do 6 ur po enkratnem odmerku zdravila Apidra in običajnem humanem insulinu. Zdravilo Apidra je bilo dano 2 minuti (Apidra - pred) pred začetkom obroka v primerjavi z običajnim humanim insulinom, ki je bilo dano 30 minut (redno - 30 min) pred začetkom obroka (slika 1A) in v primerjavi z običajnim človeškim insulinom (navaden - pred), ki je bil dan 2 minuti pred obrokom (slika 1B). Apidra je dobila 15 minut (Apidra - post) po začetku obroka v primerjavi z običajnim človeškim insulinom (rednim - pred), ki je bil dan 2 minuti pred obrokom (slika 1C). Na osi x (0) je začetek 15-minutnega obroka.
 |
 |
 |
 |
V randomizirani, odprti, dvosmerni navzkrižni študiji je 16 zdravih moških prejelo intravensko infuzija zdravila Apidra ali običajnega humanega insulina s fiziološko raztopino s hitrostjo 0,8 milijon enot / kg / min za dva ure. Infuzija istega odmerka Apidre ali navadnega humanega insulina povzroči enakovredno odstranjevanje glukoze v stanju dinamičnega ravnovesja.
Farmakokinetika
Absorpcija in biološka uporabnost
Farmakokinetični profili pri zdravih prostovoljcih in bolnikih s sladkorno boleznijo (tip 1 ali tip 2) so pokazali, da je absorpcija glulisina inzulina hitrejša kot pri običajnem človeškem insulinu.
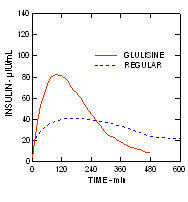
V študiji pri bolnikih s sladkorno boleznijo tipa 1 (n = 20) po subkutanem dajanju 0,15 enot / kg, srednji čas do največje koncentracije (Tmax) je bila 60 minut (razpon 40 do 120 minut) in najvišja koncentracija (Cmax) je bila 83 mikro enot / ml (razpon 40 do 131 mikro enot / ml) za insulin glulisin v primerjavi s povprečnim 120 minutnim Tmaxom (razpon 60 do 239 minut) in Cmax 50 mikro enot / ml (razpon od 35 do 71 mikro enot / ml) za navadnega človeka inzulina. (Slika 2)
Slika 2. Farmakokinetični profili insulina glulisina in običajnega humanega insulina pri bolnikih s sladkorno boleznijo tipa 1 po odmerku 0,15 enot / kg.

Insulin glulisin in običajni humani insulin so dajali subkutano v odmerku 0,2 enote / kg v anu študija evglikemične klešče pri bolnikih s sladkorno boleznijo tipa 2 (n = 24) in indeksom telesne mase (ITM) med 20 in 36 kg / m2. Mediana časa do največje koncentracije (Tmax) je bila 100 minut (razpon 40 do 120 minut), srednja največja koncentracija (Cmax) pa 84 mikro enot / ml (razpon od 53 do 165 mikro enot / ml) inzulinske glulisine v primerjavi z 240 minutno mediano Tmax (razpon 80 do 360 minut) in srednjo Cmax 41 mikro enot / ml (razpon 33 do 61 mikro enot / ml) za običajni humani insulin. (Slika 3.)
Slika 3. Farmakokinetični profili insulina glulisina in običajnega humanega insulina pri bolnikih s sladkorno boleznijo tipa 2 po subkutanem odmerku 0,2 enote / kg.
Ko so zdravilo Apidra injicirali subkutano v različna področja telesa, so bili profili časovne koncentracije podobni. Absolutna biološka uporabnost insulina glulisina po subkutanem dajanju je približno 70%, ne glede na območje injiciranja (trebuh 73%, deltoid 71%, stegno 68%).
V klinični študiji pri zdravih prostovoljcih (n = 32) je bila skupna biološka uporabnost insulina glulisina podobna po subkutanem injiciranje insulina glulisina in NPH insulina (predhodno mešanega v brizgi) in po ločenih sočasnih subkutanih injekcije. Po predhodnem mešanju je prišlo do 27% slabljenja največje koncentracije (Cmax) Apidre; vendar čas na največjo koncentracijo (Tmax) ni vplival. Podatkov o mešanju zdravila Apidra z inzulinskimi pripravki, ki niso NPH in drugi, ni na voljo. [Glej Klinične študije].
Distribucija in odprava
Porazdelitev in izločanje insulina glulisina in običajnega humanega insulina po intravenski uporabi dajanje je podobno s količino porazdelitve 13 in 21 L ter razpolovno dobo 13 in 17 minut, oz. Po subkutanem dajanju se insulin glulisin izloči hitreje kot običajni humani insulin z navidezno razpolovno dobo 42 minut v primerjavi s 86 minutami.
Klinična farmakologija pri specifičnih populacijah
Pediatrični bolniki
Farmakokinetične in farmakodinamične lastnosti zdravila Apidra in običajnega humanega insulina so bile ocenjene v a raziskava, opravljena pri otrocih od 7 do 11 let (n = 10) in mladostnikih od 12 do 16 let (n = 10) s tipom 1 diabetes. Relativne razlike v farmakokinetiki in farmakodinamiki med Apidro in običajnim humanim insulinom v ti bolniki s sladkorno boleznijo tipa 1 so bili podobni kot pri zdravih odraslih osebah in odraslih s tipom 1 diabetes.
Dirka
Študija pri 24 zdravih kavkaških in japonskih osebah je primerjala farmakokinetiko in farmakodinamiko po subkutanem injiciranju insulina glulisina, insulina lispro in običajnega humanega insulina. S subkutano injekcijo insulina glulisina so imeli japonski preiskovanci večjo začetno izpostavljenost (33%) za razmerje med AUC (0-1h) in AUC (konec 0 sponk) kot belci (21%), čeprav so bile skupne izpostavljenosti podobno. Podobne ugotovitve so bile pri insulinu lispro in običajnem humanem insulinu.
Debelost
Insulin glulisin in običajni humani insulin so dajali subkutano v odmerku 0,3 enote / kg v a študija evglikemične spone pri debelih, nediabetičnih osebah (n = 18) z indeksom telesne mase (ITM) med 30 in 40 kg / m2. Mediana časa do največje koncentracije (Tmax) je bila 85 minut (razpon 49 do 150 minut), srednja največja koncentracija (Cmax) pa je bila 192 mikro enot / ml (razpon od 98 do 380 mikro enot / ml) za insulin glulisin v primerjavi s srednjo Tmax 150 minut (razpon 90 do 240 minut) in srednjo Cmax 86 mikro enot / ml (razpon 43 do 175 mikro enot / ml) za navadnega človeka inzulina.
Hitrejši začetek delovanja in krajše trajanje aktivnosti zdravila Apidra in insulina lispro v primerjavi z običajnim človeškim insulinom sta se ohranila pri debeli populaciji, ki ni diabetična (n = 18). (Slika 4.)
Slika 4. Stopnja infuzije glukoze (GIR) v študiji evglikemičnih sponk po subkutanem injiciranju 0,3 enote / kg Apidre, insulina lispro ali običajnega humanega insulina pri debelih populacijah.
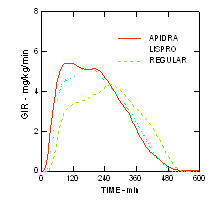
Okvara ledvic
Študije s človeškim insulinom so pokazale povečano koncentracijo insulina v obtoku pri bolnikih z odpovedjo ledvic. V študiji, opravljeni pri 24 osebah, ki niso diabetiki, z normalno ledvično funkcijo (ClCr> 80 ml / min), zmerno okvaro ledvic (30-50 ml / min) in hudo okvaro ledvic (opozorila in previdnostni ukrepi).
Okvara jeter
Vpliv okvare jeter na farmakokinetiko in farmakodinamiko zdravila Apidra niso preučevali. Nekatere študije s humanim insulinom so pokazale povečano koncentracijo insulina v obtoku pri bolnikih z odpovedjo jeter. [Glej Opozorila in previdnostni ukrepi].
Spol
Vpliv spola na farmakokinetiko in farmakodinamiko zdravila Apidra ni bil raziskan.
Nosečnost
Vpliv nosečnosti na farmakokinetiko in farmakodinamiko zdravila Apidra ni bil raziskan.
Kajenje
Vpliv kajenja na farmakokinetiko in farmakodinamiko zdravila Apidra ni bil raziskan.
vrh
Neklinična toksikologija
Kancerogeneza, mutageneza, oslabitev plodnosti
Standardne dvoletne študije rakotvornosti pri živalih niso bile izvedene. Pri podganah Sprague Dawley so izvedli 12-mesečno študijo toksičnosti za ponavljajoče odmerke z insulinom glulisin v subkutanih odmerkih 2,5, 5, 20 oz. 50 enot / kg dvakrat na dan (odmerek, ki povzroči izpostavljenost 1, 2, 8 in 20-kratnik povprečnega odmerka pri ljudeh glede na površino telesa primerjava).
Pri samskih podganah, ki so prejemale insulin glulisin, je bila od odmerka odvisna večja incidenca tumorjev mlečnih žlez v primerjavi z nezdravljenimi kontrolami. Pojavnost tumorjev mlečne žleze za insulinski glulisin in običajni humani insulin je bila podobna. Pomen teh ugotovitev za ljudi ni znan. Inzulinski glulisin ni bil mutageni pri naslednjih testih: Amesov test, in vitro sesalni kromosom aberacijski test v celicah kitajskega hrčka V79 in test in mikrožikle eritrocitov sesalcev in vivo v podgane.
V študijah plodnosti pri samcih in samicah podgan v subkutanih odmerkih do 10 enot / kg enkrat na dan (odmerek, zaradi katerega je izpostavljenost 2-krat večja od povprečnega človeka odmerek, ki temelji na primerjavi telesne površine), ni bilo jasnih škodljivih učinkov na plodnost samcev in samic ali na splošno reproduktivno sposobnost živali opazili.
vrh
Klinične študije
Varnost in učinkovitost zdravila Apidra so preučevali pri odraslih bolnikih s sladkorno boleznijo tipa 1 in tipa 2 (n = 1833) ter pri otrocih in mladostnikih (4 do 17 let) s sladkorno boleznijo tipa 1 (n = 572). Primarni parameter učinkovitosti v teh preskušanjih je bil nadzor glikemije, ocenjen z uporabo glikiranega hemoglobina (GHb je bil poročen kot ekvivalent HbA1c).
Diabetes tipa 1-odrasli
Za bolnike s sladkorno boleznijo tipa 1 je bila izvedena 26-tedenska, randomizirana, odprta, z aktivnim nadzorom, ne-inferiornost za oceno varnost in učinkovitost zdravila Apidra (n = 339) v primerjavi z insulinom lispro (n = 333), če ga dajemo subkutano v 15 minutah pred obrok. Insulin glargin so dajali enkrat dnevno zvečer kot osnovni inzulin. Pred randomizacijo je bilo obdobje uvajanja insulina lispro in insulina glargin 4 tedne. Večina bolnikov je bila kavkaška (97%). Osemdeset osem odstotkov bolnikov je bilo moških. Povprečna starost je bila 39 let (razpon od 18 do 74 let). Glikemični nadzor, število dnevnih injekcij inzulina s kratkim delovanjem ter skupni dnevni odmerki zdravila Apidra in insulina lispro so bili v obeh skupinah zdravljenja podobni (preglednica 6).
Tabela 6: Diabetes Mellitus tipa 1 - za odrasle
| Trajanje zdravljenja Zdravljenje v kombinaciji z: |
26 tednov Inzulinski glargin |
|
|---|---|---|
| Apidra | Insulin Lispro | |
| ||
| Glicirani hemoglobin (GHb)* (%) | ||
| Število bolnikov | 331 | 322 |
| Izhodiščno povprečje | 7.6 | 7.6 |
| Prilagojena srednja sprememba od osnovne | -0.1 | -0.1 |
| Razlika v zdravljenju: Apidra - Insulin Lispro | 0.0 | |
| 95% CI za razliko v zdravljenju | (-0.1; 0.1) | |
| Bazalni odmerek insulina (enote / dan) | ||
| Izhodiščno povprečje | 24 | 24 |
| Prilagojena srednja sprememba od osnovne | 0 | 2 |
| Kratko delujoči odmerek insulina (enote / dan) | ||
| Izhodiščno povprečje | 30 | 31 |
| Prilagojena srednja sprememba od osnovne | -1 | -1 |
| Povprečno število injekcij inzulina s kratkim delovanjem na dan | 3 | 3 |
| Telesna teža (kg) | ||
| Izhodiščno povprečje | 73.9 | 74.1 |
| Povprečna sprememba od osnovne | 0.6 | 0.3 |
Diabetes tipa 2-odrasli
Za bolnike, ki so zdravili z insulinom s sladkorno boleznijo tipa 2, so izvedli 26-tedensko, randomizirano, odprto, z aktivnim nadzorom ne-inferiornosti študijo za oceno varnost in učinkovitost zdravila Apidra (n = 435), ki se daje v 15 minutah pred obrokom, v primerjavi z običajnim človeškim insulinom (n = 441), ki se daje 30 do 45 minut pred obrok. Človeški inzulin NPH je bil dodeljen dvakrat na dan kot osnovni insulin. Vsi pacienti so sodelovali v obdobju 4 tednov potek običajnega humanega insulina in humanega insulina NPH. Osemindvajset odstotkov bolnikov je bilo kavkaških, 11 odstotkov pa črnopoltih. Povprečna starost je bila 58 let (razpon od 26 do 84 let). Povprečni indeks telesne mase (BMI) je bil 34,6 kg / m2. Po randomizaciji je 58% bolnikov jemalo peroralno antidiabetično sredstvo. Ti bolniki so bili poučeni, naj nadaljujejo z uporabo peroralnega antidiabetičnega zdravila v istem odmerku skozi celotno preskušanje. Večina bolnikov (79%) je pomešala svoj kratko delujoči inzulin s človeškim insulinom NPH tik pred injiciranjem. Znižanja izhodiščne vrednosti GHb so bila podobna med dvema skupinama zdravljenja (glejte tabelo 7). Pri številu dnevnih injekcij inzulina s kratkim delovanjem ali bazalnih ali kratkodelujočih odmerkih insulina niso opazili razlik med skupinami Apidra in navadnih humanih insulinov. (Glej tabelo 7.)
Tabela 7: Diabetes Mellitus-Adult 2
| Trajanje zdravljenja | 26 tednov | |
|---|---|---|
| Zdravljenje v kombinaciji z: | NPH humani insulin | |
| Apidra | Redni človeški inzulin | |
| ||
| Glicirani hemoglobin (GHb)* (%) | ||
| Število bolnikov | 404 | 403 |
| Izhodiščno povprečje | 7.6 | 7.5 |
| Prilagojena srednja sprememba od osnovne | -0.5 | -0.3 |
| Razlika v zdravljenju: Apidra - redni humani inzulin | -0.2 | |
| 95% CI za razliko v zdravljenju | (-0.3; -0.1) | |
| Bazalni odmerek insulina (enote / dan) | ||
| Izhodiščno povprečje | 59 | 57 |
| Prilagojena srednja sprememba od osnovne | 6 | 6 |
| Kratko delujoči odmerek insulina (enote / dan) | ||
| Izhodiščno povprečje | 32 | 31 |
| Prilagojena srednja sprememba od osnovne | 4 | 5 |
| Povprečno število injekcij inzulina s kratkim delovanjem na dan | 2 | 2 |
| Telesna teža (kg) | ||
| Izhodiščno povprečje | 100.5 | 99.2 |
| Povprečna sprememba od osnovne | 1.8 | 2.0 |
Sladkorna bolezen tipa 1: Odmerjanje pred in po obroku
Izvedena je bila 12-tedenska, randomizirana, odprta, z aktivnim nadzorom ne-inferiornost študija pri bolnikih z sladkorna bolezen tipa 1 za oceno varnosti in učinkovitosti zdravila Apidra, ki se daje v različnih obdobjih glede na a obrok. Apidro so dajali subkutano bodisi v 15 minutah pred obrokom (n = 286) bodisi takoj po a obrok (n = 296) in običajni humani inzulin (n = 278) so dajali subkutano 30 do 45 minut pred obrok. Insulin glargin so dajali enkrat na dan pred spanjem kot osnovni inzulin. V obdobju običajnega humanega insulina in inzulina glargin je sledilo 4-tedensko obdobje, ki mu je sledila randomizacija. Večina bolnikov je bila kavkaška (94%). Povprečna starost je bila 40 let (razpon od 18 do 73 let). Glikemična kontrola (glej preglednico 8) je bila primerljiva za 3 sheme zdravljenja. Pri skupnem dnevnem številu injekcij inzulina s kratkotrajnim delovanjem ni bilo sprememb glede na izhodišče med zdravljenjem. (Glej tabelo 8.)
Tabela 8: Uporaba pred in po obroku pri diabetesu mellitus-Adult tipa 1
| Trajanje zdravljenja Zdravljenje v kombinaciji z: |
12 tednov inzulin glargin |
12 tednov inzulin glargin |
12 tednov inzulin glargin |
|---|---|---|---|
| Apidra pred obrokom |
Apidra post obrok |
Redni človeški inzulin | |
| |||
| Glicirani hemoglobin (GHb)* (%) | |||
| Število bolnikov | 268 | 276 | 257 |
| Izhodiščno povprečje | 7.7 | 7.7 | 7.6 |
| Prilagojena srednja sprememba od osnovne†| -0.3 | -0.1 | -0.1 |
| Bazalni odmerek insulina (enote / dan) | |||
| Izhodiščno povprečje | 29 | 29 | 28 |
| Prilagojena srednja sprememba od osnovne | 1 | 0 | 1 |
| Kratko delujoči odmerek insulina (enote / dan) | |||
| Izhodiščno povprečje | 29 | 29 | 27 |
| Prilagojena srednja sprememba od osnovne | -1 | -1 | 2 |
| Povprečno število injekcij inzulina s kratkim delovanjem na dan | 3 | 3 | 3 |
| Telesna teža (kg) | |||
| Izhodiščno povprečje | 79.2 | 80.3 | 78.9 |
| Povprečna sprememba od osnovne | 0.3 | -0.3 | 0.3 |
Diabetični bolniki tipa 1
Izvedena je bila 26-tedenska, randomizirana, odprta, z aktivnim nadzorom ne-inferiornosti študija pri otrocih in mladostnikih, starejših od 4 let s tipom 1 diabetes mellitus za oceno varnosti in učinkovitosti zdravila Apidra (n = 277) v primerjavi z insulinom lispro (n = 295), če ga dajemo subkutano v 15 minutah pred obrok. Bolniki so prejemali tudi insulin glargin (ki ga dajemo enkrat dnevno zvečer) ali insulin NPH (ki ga dajemo enkrat zjutraj in enkrat zvečer). Pred randomizacijo je prišlo do 4-tedenskega obdobja uvajanja insulina lispro in insulina glargin ali NPH. Večina bolnikov je bila kavkaška (91%). Petdeset odstotkov bolnikov je bilo moškega spola. Povprečna starost je bila 12,5 let (razpon od 4 do 17 let). Povprečni BMI je znašal 20,6 kg / m2. Glikemična kontrola (glej preglednico 9) je bila primerljiva za dva režima zdravljenja.
Tabela 9: Rezultati 26-tedenske študije pri otrocih z diabetesom mellitusom tipa 1
| Apidra | Lispro | |
|---|---|---|
| Število bolnikov | 271 | 291 |
| Bazalni inzulin | NPH ali insulin glargin | NPH ali insulin glargin |
| ||
| Glicirani hemoglobin (GHb)* (%) | ||
| Izhodiščno povprečje | 8.2 | 8.2 |
| Prilagojena srednja sprememba od osnovne | 0.1 | 0.2 |
| Razlika med zdravljenjem: povprečna (95-odstotni interval zaupanja) | -0.1 (-0.2, 0.1) | |
| Bazalni odmerek insulina (enote / kg / dan) | ||
| Izhodiščno povprečje | 0.5 | 0.5 |
| Povprečna sprememba od osnovne | 0.0 | 0.0 |
| Kratko delujoči odmerek insulina (enote / kg / dan) | ||
| Izhodiščno povprečje | 0.5 | 0.5 |
| Povprečna sprememba od osnovne | 0.0 | 0.0 |
| Povprečno število injekcij inzulina s kratkim delovanjem na dan | 3 | 3 |
| Izhodiščna srednja telesna teža (kg) | 51.5 | 50.8 |
| Povprečna sprememba teže od osnovne (kg) | 2.2 | 2.2 |
Sladkorna bolezen tipa 1: Stalna podkožna infuzija insulina
12-tedenska randomizirana aktivna kontrolna študija (Apidra proti insulinu aspart), izvedena pri odraslih s sladkorno boleznijo tipa 1 (Apidra n = 29, inzulin aspart n = 30) so ocenili uporabo zdravila Apidra v zunanjem neprekinjenem podkožnem insulinu črpalka. Vsi bolniki so bili kavkaški. Povprečna starost je bila 46 let (razpon od 21 do 73 let). V obeh skupinah zdravljenja se je povprečni GHb od začetne do končne točke povečal (s 6,8% na 7,0% za zdravilo Apidra; od 7,1% do 7,2% za inzulin aspart).
vrh
Kako dobava / skladiščenje in ravnanje
Kako dobavljeno
| |
| Apidra 100 enot na ml (U-100) je na voljo kot: | |
| 10 ml viale | NDC 0088-2500-33 |
| 3 ml sistem kartuš*, paket 5 | NDC 0088-2500-52 |
| 3 ml napolnjeni injekcijski peresnik SoloStar, paket 5 | NDC 0088-2502-05 |
Igle za pero niso vključene v pakiranjih.
Igle za peresnike BD Ultra-Fine ™1, ki jih uporabljamo skupaj z OptiClikom, se prodajajo ločeno, izdelujejo pa jih Becton Dickinson in Company.
Solostar je združljiv z vsemi injekcijskimi iglami iz Becton Dickinson and Company, Ypsomed in Owen Mumford.
Skladiščenje
Ne uporabljajte po datumu uporabnosti (glejte škatlo in posodo).
Neodprti sistem viale / kartuše / SoloStar
Neodprte viale Apidra, sistem kartuš in SoloStar je treba hraniti v hladilniku (2 ° C-8 ° C), 36 ° F-46 ° F. Zaščititi pred svetlobo. Zdravila Apidra ne smete shranjevati v zamrzovalniku in ga ne smete zamrzovati. Zavrzite, če je bil zamrznjen.
Neodprte viale / sisteme kartuš / SoloStar, ki niso shranjene v hladilniku, je treba uporabiti v 28 dneh.
Odprta (med uporabo) viala:
Odprte viale, ohlajene ali ne, je treba uporabiti v 28 dneh. Če hlajenje ni mogoče, lahko odprto vialo shranjujete v hladilniku do 28 dni, oddaljeno od neposredne toplote in svetlobe, dokler temperatura ni višja od 25 ° C (77 ° F).
Odprti (v uporabi) sistem kartuš:
Odprtega sistema (v uporabi) kartuše, vstavljenega v OptiClik®, NE smete hladiti, ampak ga hraniti pod (25 ° C) oddaljenim od neposredne toplote in svetlobe. Odprti (v uporabi) sistem kartuš morate po 28 dneh zavreči. OptiClik® s sistemom kartuš ne shranjujte v hladilniku kadar koli.
Odprto (v uporabi) napolnjeno injekcijsko pero SoloStar:
Odprtega (v uporabi) SoloStarja NE smete hladiti, ampak ga hraniti pod (25 ° C) pod temperaturo 77 ° F (neposredna toplota in svetloba). Odprto (v uporabi) SoloStar, hranjeno pri sobni temperaturi, je treba po 28 dneh zavreči.
Infuzijski seti:
Infuzijske komplete (rezervoarje, cevke in katetre) in Apidro v rezervoarju je treba zavreči po 48 urah uporabe ali po izpostavljenosti 37 ° C temperaturam, ki presegajo 98,6 ° F.
Intravenska uporaba:
Infuzijske vrečke, pripravljene, kot je navedeno pod ODDELEK IN UPORABA so stabilne pri sobni temperaturi 48 ur.
Priprava in ravnanje
Po razredčenju za intravensko uporabo je treba raztopino pred uporabo vizualno pregledati, ali vsebuje delce in razbarvanje. Ne uporabljajte raztopine, če je postala motna ali vsebuje delce; uporabljajte le, če je bistra in brezbarvna. Apidra ni združljiva z raztopino Dekstroze in raztopine Ringerja, zato je ni mogoče uporabiti s temi raztopinami. Uporaba zdravila Apidra z drugimi raztopinami ni bila raziskana, zato je odsvetujemo.
Kartušni sistem: Če OptiClik® (naprava za dovajanje insulina za Apidro) ne deluje, lahko Apidra iz sistema kartuše potegnete v brizgo U-100 in jo injicirate.
Apidra, insulin glusin, podatki o bolniku (v navadni angleščini)
nazadnje posodobljeno: 02/2009
Podrobne informacije o znakih, simptomih, vzrokih, zdravljenju sladkorne bolezni
Informacije v tej monografiji ne zajemajo vseh možnih načinov uporabe, navodil, previdnostnih ukrepov, interakcij z zdravili ali škodljivih učinkov. Te informacije so posplošene in niso mišljene kot poseben zdravniški nasvet. Če imate vprašanja o zdravilih, ki jih jemljete ali bi želeli več informacij, se posvetujte s svojim zdravnikom, farmacevtom ali medicinsko sestro.
nazaj k: Preglejte vsa zdravila za zdravljenje sladkorne bolezni



