Iloperidon (fanapt) Celotne informacije o predpisovanju
Blagovna znamka: Fanapt
Splošno ime: Iloperidon
Priročnik za predpisovanje zdravila Fanapt (Iloperidon) (PDF)
Vsebina:
Opozorilno sporočilo
Indikacije in uporaba
Odmerjanje in uporaba
Kontraindikacije
Opozorila in previdnostni ukrepi
Neželeni učinki
Interakcije z zdravili
Uporaba v specifičnih populacijah
Zloraba drog in odvisnost
Predoziranje
Opis
Klinična farmakologija
Neklinična toksikologija
Klinične študije
Kako dobavljeno
Vodnik za zdravila Brintellix
OPOZORILO: POVEČANA MORTALNOST PRI REDNIH PACIENTIH Z DIHEZIJO, POROČENO PSIHOZO
Pri starejših bolnikih z demenco, povezano s psihozo, zdravljenih z antipsihotiki, obstaja večje tveganje za smrt. Zdravilo FANAPT ni odobreno za zdravljenje bolnikov z demenco, povezano s psihozo.
Indikacije in uporaba
FANAPT® je indiciran za zdravljenje shizofrenije pri odraslih.
Pri odločanju med alternativnimi načini zdravljenja za to stanje mora zdravnik predpisovati ugotovitev, da je FANAPT povezan s podaljšanjem intervala QTc. Podaljšanje intervala QTc je povezano z nekaterimi drugimi zdravili, ki lahko povzročijo torsade de aritmija tipa pointes, potencialno usodna polimorfna ventrikularna tahikardija, ki lahko povzroči nenadno smrt. V mnogih primerih bi to privedlo do zaključka, da je treba najprej poskusiti druga zdravila. Ali bo FANAPT povzročil torsade de pointes ali povečal stopnjo nenadne smrti, še ni znano.
Bolnike je treba titrirati do učinkovitega odmerka zdravila FANAPT. Tako se lahko nadzor nad simptomi odloži v prvih 1 do 2 tednih zdravljenja v primerjavi z nekaterimi drugimi antipsihotiki, ki ne potrebujejo podobne titracije. Pri izbiri antipsihotičnega zdravila za zdravljenje shizofrenije morajo zdravniki upoštevati to zamudo.
nadaljevanje zgodbe spodaj
Odmerjanje in uporaba
Običajna doza
Zdravilo FANAPT je treba počasi titrirati od nizkega začetnega odmerka, da se prepreči ortostatska hipotenzija zaradi blokatorskih lastnosti alfa-adrenergikov. Priporočeni začetni odmerek za tablete FANAPT je 1 mg peroralno dvakrat na dan. Povečanje odmerka, da dosežemo ciljno območje 6 -12 mg dvakrat na dan (12_24 mg / dan), je mogoče izvesti z dnevnimi prilagoditvami odmerkov, ki ne presegajo 2 mg dvakrat na dan (4 mg / dan). Največji priporočeni odmerek je 12 mg dvakrat na dan (24 mg / dan). V kliničnih preskušanjih odmerkov zdravila FANAPT nad 24 mg / dan niso sistematično ocenjevali. Učinkovitost je bila dokazana s FANAPT v odmerku od 6 do 12 mg dvakrat na dan. Naročniki se morajo zavedati dejstva, da je treba bolnike titrirati do učinkovitega odmerka zdravila FANAPT. Tako se lahko nadzor nad simptomi odloži v prvih 1 do 2 tednih zdravljenja v primerjavi z nekaterimi drugimi antipsihotiki, ki ne potrebujejo podobne titracije. Naročniki se morajo zavedati tudi, da so nekateri škodljivi učinki, povezani z uporabo FANAPT, odvisni od odmerka. Zdravilo FANAPT se lahko daje ne glede na obroke.
Odmerjanje v posebnih populacijah
Prilagoditev odmerka za bolnike, ki jemljejo zdravilo FANAPT sočasno s potencialnimi zaviralci CYP2D6: Odmerek FANAPT naj bo zmanjšano za polovico, če ga dajemo sočasno z močnimi zaviralci CYP2D6, kot so fluoksetin ali paroksetin. Ko se zaviralec CYP2D6 umakne iz kombiniranega zdravljenja, je treba odmerek FANAPT povečati na mesto, kjer je bil prej.
Prilagoditev odmerka za bolnike, ki jemljejo zdravilo FANAPT sočasno s potencialnimi zaviralci CYP3A4: Odmerek FANAPT naj bo zmanjšano za polovico, če ga dajemo sočasno z močnimi zaviralci CYP3A4, kot je ketokonazol oz. klaritromicin. Ko se zaviralec CYP3A4 umakne iz kombiniranega zdravljenja, je treba odmerek FANAPT povečati tam, kjer je bil prej.
Prilagoditev odmerka za bolnike, ki jemljejo FANAPT, ki so slabi metabolizatorji CYP2D6: Pri slabih metabolizatorjih CYP2D6 je treba odmerek FANAPT zmanjšati za polovico.
Okvara jeter: Pri bolnikih z blago jetrno okvaro odmerka FANAPT ni treba prilagajati. Bolniki z zmerno okvaro jeter lahko zahtevajo zmanjšanje odmerka, če je to klinično indicirano. Zdravila FANAPT ne priporočamo bolnikom s hudo okvaro jeter.
Vzdrževalno zdravljenje
V dolgotrajnejši študiji je bil zdravilo FANAPT učinkovito pri odlašanju časa za ponovitev pri bolnikih s shizofrenijo, ki so bili stabilizirani na FANAPT do 24 mg / dan. Bolnike je treba redno ocenjevati, da se ugotovi potreba po vzdrževalnem zdravljenju.
Ponovna prekinitev zdravljenja pri bolnikih, ki so jih prej prekinili Čeprav ni podatkov, ki bi posebej obravnavali ponovno zdravljenje z zdravili Za zdravljenje je priporočljivo upoštevati shemo začetne titracije, kadar so imeli pacienti več intervala FANAPT kot 3 dni.
vrh
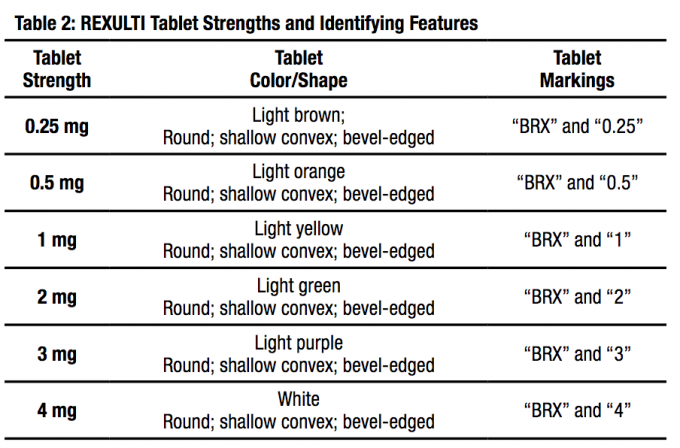
Odmerne oblike in jakosti
FANAPT tablete so na voljo v naslednjih jakostih: 1 mg, 2 mg, 4 mg, 6 mg, 8 mg, 10 mg in 12 mg. Tablete so bele, okrogle, ploščate, s poševnimi robovi in označene z logotipom "", vtisnjenim na eni strani in s tabletami "1", "2", "4", "6", "8", "10", ali "12", vtisnjeno na drugi strani.
vrh
Kontraindikacije
Zdravilo FANAPT je kontraindicirano pri osebah z znano reakcijo preobčutljivosti na zdravilo. Poročali so o anafilaksiji, angioedemu in drugih preobčutljivostnih reakcijah.
vrh
OPOZORILA IN VARNOSTNI UKREPI
Povečana umrljivost pri starejših bolnikih z demenco povezano psihozo
Antipsihotična zdravila povečajo tveganje smrti pri starejših bolnikih z demenco, povezano s psihozo. Analize 17 bolnikov z demenco, povezanih s placebo, s placebom nadzorovanih preskušanj (modalno trajanje 10 tednov in večinoma pri bolnikih, ki so jemali atipično antipsihotiki) so pri bolnikih, ki so jih zdravili, odkrili tveganje smrti med 1,6 do 1,7-krat večjim kot pri bolnikih, ki so prejemali placebo. Med značilnim 10-tedenskim nadzorovanim preskušanjem je bila stopnja smrti pri bolnikih, zdravljenih z zdravili, približno 4,5%, v primerjavi s stopnjo približno 2,6% pri bolnikih, ki so prejemali placebo.
Čeprav so bili vzroki smrti različni, je bila večina smrti v naravi bodisi srčno-žilna (npr. Srčno popuščanje, nenadna smrt) bodisi nalezljiva (npr. Pljučnica). Zdravilo FANAPT ni odobreno za zdravljenje bolnikov z demenco, povezano s psihozo.
Cerebrovaskularni neželeni učinki, vključno z možgansko kapjo pri starejših bolnikih z demenco povezano psihozo
V placebo nadzorovanih preskušanjih pri starejših osebah z demenco so bili bolniki, randomizirani na risperidon, aripiprazol in olanzapin sta imeli pogostejšo možgansko kap in prehodni ishemični napad, vključno s smrtnim kap. Zdravilo FANAPT ni odobreno za zdravljenje bolnikov z demenco, povezano s psihozo.
Podaljšanje QT
V odprti študiji QTc pri bolnikih s shizofrenijo ali shizoafektivno motnjo (n = 160) je bil FANAPT povezan s podaljšanjem QTc za 9 msec pri odmerku iloperidona 12 mg dvakrat na dan. Učinek zdravila FANAPT na interval QT je bil povečan s prisotnostjo presnovne inhibicije CYP450 2D6 ali 3A4 (paroksetin 20 mg enkrat na dan in ketokonazol 200 mg dvakrat na dan). Pod pogoji zaviranja presnove za 2D6 in 3A4 je bil FANAPT 12 mg dvakrat na dan povezan s povprečnim povečanjem QTcF od izhodiščne vrednosti približno 19 msec.
Med kliničnim programom pred trženjem niso opazili primerov torsade de pointes ali drugih hudih srčnih aritmij.
Izogibati se je treba uporabi zdravila FANAPT v kombinaciji z drugimi zdravili, za katera je znano, da podaljšujejo QTc, vključno s razredom 1A (npr. Kinidin, prokainamid) ali antiaritmičnih zdravil razreda III (npr. amiodarona, sotalola), antipsihotičnih zdravil (npr. klorpromazin, tioridazin), antibiotikov (npr. gatifloksacin, moksifloksacin) ali katero koli drugo vrsto zdravil, za katere je znano, da podaljšajo interval QTc (npr. pentamidin, levomethalacetat, metadon). Izogibati se je treba FANAPT tudi pri bolnikih s prirojenim dolgim QT sindromom in pri bolnikih z anamnezo srčne aritmije.
Nekatere okoliščine lahko povečajo tveganje za nastanek torsade de pointes in / ali nenadno smrt v povezavi z uporabo zdravil, ki podaljšajo interval QTc, vključno z (1) bradikardijo; (2) hipokalemija ali hipomagnezijemija; (3) sočasna uporaba drugih zdravil, ki podaljšujejo interval QTc; in (4) prisotnost prirojenega podaljšanja intervala QT; (5) nedavni akutni miokardni infarkt; in / ali (6) kompenzirano srčno popuščanje.
Pri predpisovanju zdravila FANAPT z zdravili, ki zavirajo presnovo FANAPT, in pri bolnikih z zmanjšano aktivnostjo CYP2D6 je potrebna previdnost.
Priporočljivo je, da se pri zdravljenju z zdravilom FANAPT obravnavajo bolniki, pri katerih obstaja velika nevarnost elektrolitske motnje imajo izhodiščne meritve kalija in magnezija v serumu s periodičnimi meritvami spremljanje. Hipokalemija (in / ali hipomagneziemija) lahko poveča tveganje za podaljšanje QT in aritmijo. FANAPT se je treba izogniti bolnikom z zgodovino pomembnih srčno-žilnih bolezni, na primer QT podaljšanje, nedavni akutni miokardni infarkt, kompenzirano srčno popuščanje ali srčna aritmija. Pri bolnikih, za katere se ugotovi, da imajo trajne meritve QTc> 500 msec, je treba FANAPT ukiniti.
Če imajo bolniki, ki jemljejo zdravilo FANAPT, simptome, ki bi lahko kazali na pojav srčnih aritmij, npr. omotico, palpitacije ali sinkopo, mora predpisovalec začeti nadaljnjo oceno, vključno s srčno spremljanje.
Nevroleptični maligni sindrom (NMS)
V povezavi z dajanjem antipsihotičnih zdravil, vključno s FANAPT, so poročali o možno smrtnem kompleksnem simptomu, ki ga včasih imenujejo nevroleptični maligni sindrom (NMS). Klinične manifestacije vključujejo hiperpireksijo, mišično togost, spremenjeno duševno stanje (vključno s katatoničnimi znaki) in dokazi o avtonomni nestabilnosti (nepravilen pulz ali krvni tlak, tahikardija, diaforeza in srčna bolezen disitmija). Dodatni znaki lahko vključujejo povišano kreatin fosfokinazo, mioglobinurijo (rabdomioliza) in akutno odpoved ledvic. Diagnostična ocena bolnikov s tem sindromom je zapletena. Pri postavitvi diagnoze je pomembno prepoznati primere, v katerih je vključena tudi klinična predstavitev tako resne zdravstvene bolezni kot nezdravljenih ali neustrezno zdravljenih ekstrapiramidnih znakov in simptomov (EPS). Drugi pomembni vidiki diferencialne diagnoze vključujejo centralno antiholinergično toksičnost, vročinski udar, vročino z zdravili in patologijo primarnega osrednjega živčevja.
Obvladovanje tega sindroma mora vključevati: (1) takojšnjo ukinitev antipsihotikov in drugih zdravil, ki niso nujna za sočasno zdravljenje, (2) intenzivno simptomatsko zdravljenje in zdravstveno spremljanje ter (3) zdravljenje vseh sočasnih resnih zdravstvenih težav, za katere so na voljo posebna zdravljenja. Glede specifičnih režimov farmakološkega zdravljenja za NMS ni splošnega dogovora.
Če bolnik po okrevanju od NMS potrebuje zdravljenje z antipsihotiki, je treba skrbno razmisliti o morebitni ponovni uvedbi zdravljenja z zdravili. Bolnika je treba skrbno nadzorovati, saj so poročali o ponovitvah NMS.
Tardivna diskinezija
Tardivna diskinezija je sindrom, ki je sestavljen iz potencialno nepovratnih, neprostovoljnih, diskinetičnih gibanj, ki se lahko razvijejo pri bolnikih, zdravljenih z antipsihotičnimi zdravili. Čeprav je razširjenost sindroma najvišja med starejšimi, zlasti starejšimi ženskami, je nemogoče se zanašajo na ocene razširjenosti, da bodo ob začetku antipsihotičnega zdravljenja napovedovali, pri katerih bolnikih se bo verjetno razvilo sindrom. Ali se antipsihotična zdravila razlikujejo po možnosti, da povzročijo tardivno diskinezijo, ni znano.
Verjamejo tveganje za razvoj tardivne diskinezije in verjetnost, da bo postala nepopravljiva povečati kot trajanje zdravljenja in skupni kumulativni odmerek danega antipsihotika povečuje. Sindrom pa se lahko razvije, čeprav precej redkeje, po razmeroma kratkih obdobjih zdravljenja z majhnimi odmerki.
Za ugotovljene primere tardivne diskinezije ni znanega zdravljenja, čeprav se lahko sindrom delno ali v celoti odpravi, če se antipsihotično zdravljenje umakne. Samo antipsihotično zdravljenje pa lahko zavira (ali delno zavira) znake in simptome sindroma in s tem morda prikrije osnovni proces. Učinek, ki ga ima simptomatska supresija na dolgotrajen potek sindroma, ni znan.
Glede na te pomisleke je treba zdravilo FANAPT predpisati na način, ki najverjetneje zmanjša pojav tardivne diskinezije. Kronično antipsihotično zdravljenje mora biti običajno rezervirano za bolnike, ki trpijo za kronično boleznijo, na katero (1) je znano, da se odziva antipsihotiki in (2), za katera niso na voljo alternativna, enako učinkovita, vendar potencialno manj škodljiva zdravljenja ali primerno. Pri bolnikih, ki potrebujejo kronično zdravljenje, je treba iskati najmanjši odmerek in najkrajše trajanje zdravljenja, ki dajejo zadovoljiv klinični odziv. Potrebe po nadaljevanju zdravljenja je treba občasno ponovno ocenjevati.
Če se pri bolniku na FANAPT pojavijo znaki in simptomi tardivne diskinezije, je treba razmisliti o ukinitvi zdravil. Kljub temu pa nekateri bolniki kljub prisotnosti sindroma morda potrebujejo zdravljenje z zdravilom FANAPT.
Presnovne spremembe
Atipična antipsihotična zdravila so bila povezana s presnovnimi spremembami, ki lahko povečajo tveganje za srčno-žilno / cerebrovaskularno delovanje. Te presnovne spremembe vključujejo hiperglikemijo, dislipidemijo in povečanje telesne teže. Medtem ko je bilo dokazano, da vsa netipična antipsihotična zdravila povzročajo nekatere presnovne spremembe, ima vsako zdravilo v svojem razredu poseben profil tveganja.
Hiperglikemija in diabetes mellitus
Pri bolnikih, ki se zdravijo z atipičnimi antipsihotiki, vključno s FANAPT, so poročali o hiperglikemiji, ki je v nekaterih primerih ekstremna in povezana s ketoacidozo ali hiperosmolarno komo ali smrtjo. Ocenjevanje razmerja med netipičnimi antipsihotičnimi zdravili in nepravilnostmi glukoze je zapleteno zaradi možnosti večjega osnovno tveganje za nastanek diabetes mellitusa pri bolnikih s shizofrenijo in naraščajoča pojavnost diabetesa mellitusa na splošno populacija. Glede na te zmede razmerje med netipičnimi antipsihotičnimi zdravili in neželenimi učinki, povezanimi s hiperglikemijo, ni popolnoma razjasnjeno. Vendar pa epidemiološke študije kažejo na povečano tveganje za pojav neželenih učinkov hiperglikemije pri bolnikih, zdravljenih z netipičnimi antipsihotiki, vključenimi v te študije.
Bolnike z uveljavljeno diagnozo diabetes mellitus, ki so začeli z atipičnimi antipsihotiki, je treba redno spremljati, da se poslabša kontrola glukoze. Bolniki z dejavniki tveganja za diabetes mellitus (npr. Debelost, družinska anamneza sladkorne bolezni), ki se začnejo zdraviti z atipični antipsihotiki bi morali na začetku zdravljenja in občasno med zdravljenjem opraviti testiranje glukoze v krvi na tešče zdravljenje. Vsakega bolnika, ki se zdravi z atipičnimi antipsihotiki, je treba spremljati zaradi simptomov hiperglikemije, vključno s polidipsijo, poliurijo, polifagijo in šibkostjo. Bolniki, ki med zdravljenjem z atipičnimi antipsihotiki razvijejo simptome hiperglikemije, morajo opraviti testiranje glukoze v krvi na tešče. V nekaterih primerih se je hiperglikemija razrešila ob ukinitvi netipičnega antipsihotika; vendar so nekateri bolniki kljub prekinitvi sumljivega zdravila potrebovali nadaljevanje protidiabetičnega zdravljenja.
Podatki iz 4-tedenske študije s fiksnimi odmerki pri odraslih osebah s shizofrenijo, v kateri so bili odvzeti vzorci krvi na tešče, so predstavljeni v preglednici 1.
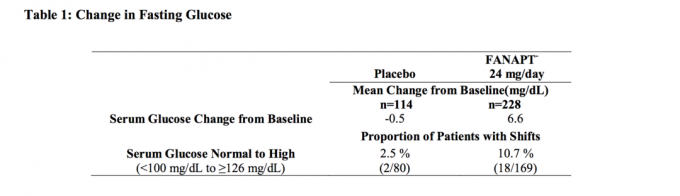
Združene analize podatkov o glukozi iz kliničnih študij, vključno z dolgoročnimi preskušanji, so prikazane v preglednici2.
Dislipidemija
Pri bolnikih, zdravljenih z atipičnimi antipsihotiki, so opazili neželene spremembe lipidov.
Podatki raziskave s 4-tedenskimi študijami s fiksnim odmerkom, pri kateri so odvzeli vzorce krvi na tešče, pri odraslih osebah s shizofrenijo so predstavljeni v preglednici 3.

Združene analize podatkov o holesterolu in trigliceridih iz kliničnih študij, vključno z dolgoročnimi preskušanji, so prikazane v preglednicah 4 in tabeli 5.
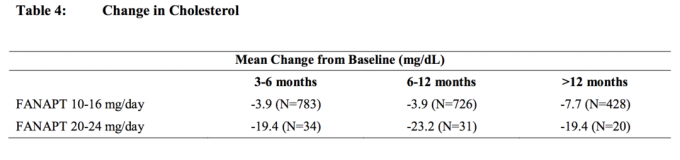
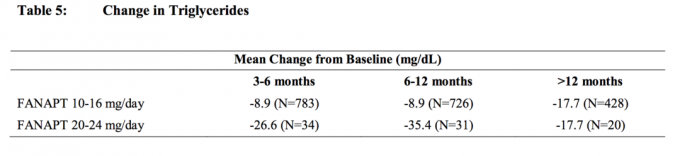
Povečanje telesne mase
Pri netipičnih antipsihotikih so opazili povečanje telesne mase. Priporočljivo je klinično spremljanje teže.
V vseh kratkoročnih in dolgoročnih študijah je bila skupna povprečna sprememba glede na izhodiščno vrednost 2,1 kg.
Spremembe telesne teže (kg) in deleža oseb z ≥7% povečanja telesne teže od 4 v placebo nadzorovanih študijah s fiksnim ali fleksibilnim odmerkom pri odraslih osebah s 4- ali 6-tedensko terapijo so predstavljeni v Tabela 6.

Epileptični napadi
V kratkotrajnih placebo nadzorovanih preskušanjih (od 4 do 6 tednov) so se napadi pojavili pri 0,1% (1/1344) bolnikov, zdravljenih s FANAPT, v primerjavi z 0,3% (2/587) pri placebu. Kot pri drugih antipsihotikih je treba tudi FANAPT previdno uporabljati pri bolnikih z napadi v anamnezi ali s stanji, ki potencialno znižajo prag napadov. Pogoji, ki znižujejo prag zasega, so lahko bolj razširjeni pri populaciji, stari 65 let ali več.
Ortostatska hipotenzija in sinkopa
Zdravilo FANAPT lahko povzroči ortostatsko hipotenzijo, povezano z omotico, tahikardijo in sinkopo. To kaže na njegove lastnosti antagonista alfa1-adrenergike. V dvojno slepih kratkoročnih študijah, nadzorovanih s placebom, kjer so odmerek počasi povečevali, kot je priporočeno zgoraj so poročali o sinkopi pri 0,4% (5/1344) bolnikov, ki so se zdravili z zdravilom FANAPT, v primerjavi z 0,2% (1/587) na placebo. O ortostatski hipotenziji so poročali pri 5% bolnikov, ki so prejemali 20-24 mg / dan, 3% bolnikov, ki so dobivali 10-16 mg / dan, in 1% bolnikov, ki so dobivali placebo. Hitrejša titracija naj bi povečala stopnjo ortostatske hipotenzije in sinkopa.
Zdravilo FANAPT je treba uporabljati previdno pri bolnikih z znano srčno-žilno boleznijo (npr. Srčno popuščanje, anamneza miokarda, anamneza in ishemija ali prevodnost nepravilnosti), cerebrovaskularno bolezen ali stanja, ki bolnika predpostavljajo hipotenzijo (dehidracija, hipovolemija in zdravljenje z antihipertenzivom zdravila). Pri bolnikih, ki so izpostavljeni hipotenziji, je treba upoštevati spremljanje ortostatskih vitalnih znakov.
Levkopenija, nevtropenija in agranulocitoza
V kliničnih preskušanjih in postmarketinških izkušnjah so poročali o dogodkih levkopenije / nevtropenije, ki so časovno povezani z antipsihotiki. Poročali so tudi o agranulocitozi (vključno s smrtnimi primeri).
Možni dejavniki tveganja za levkopenijo / nevtropenijo vključujejo predhodno nizko število belih krvnih celic (WBC) in anamnezo levkopenije / nevtropenije v anamnezi. Pri bolnikih z že obstoječo nizko koncentracijo WBC ali anamnezo levkopenije / nevtropenije v anamnezi je treba spremljati celotno krvno sliko (CBC) pogosto v prvih mesecih zdravljenja, zato je treba FANAPT prekiniti ob prvih znakih upada WBC, če ni drugih povzročiteljev dejavniki.
Bolnike z nevtropenijo je treba skrbno nadzirati zaradi vročine ali drugih simptomov ali znakov okužbe in jih nemudoma zdraviti, če se pojavijo takšni simptomi ali znaki. Bolniki s hudo nevtropenijo (absolutno število nevtrofilcev <1000 / mm3) morajo prenehati jemati zdravilo FANAPT in jim slediti, dokler ne okrevajo.
Hiperprolaktinemija
Tako kot druga zdravila, ki antagonizirajo receptorje dopamina D2, tudi FANAPT zviša raven prolaktina.
Hiperprolaktinemija lahko zavira hipotalamični GnRH, kar ima za posledico zmanjšano izločanje gonadotropina hipofize. To pa lahko zavira reproduktivno funkcijo z motenjem gonadalsteroidogeneze tako pri ženskah kot pri moških. Pri spojinah, ki dvigajo prolaktin, so poročali o galaktoreji, amenoreji, ginekomastiji in impotenci. Dolgotrajna hiperprolaktinemija, povezana s hipogonadizmom, lahko pri ženskah in moških privede do zmanjšanja kostne gostote.
Poskusi s tkivno kulturo kažejo, da je približno tretjina raka na dojki človeka in vitro odvisna od prolaktina, a dejavnik potencialnega pomena, če se pri bolniku z že odkritimi dojkami razmišlja o predpisovanju teh zdravil raka. Pri miših in podganah, zdravljenih s FANAPT, so opazili proliferativne spremembe in povečanje serumskega prolaktina v mlečnih žlezah. Niti klinične študije niti epidemiološke študije, ki so bile opravljene do danes, niso pokazale povezave med kroničnim dajanjem tega razreda zdravil in tumorigenezo pri ljudeh; razpoložljivi dokazi se trenutno štejejo za preveč omejene, da bi bili dokončni.
V kratkoročnem preskušanju s placebom (4 tedne) se povprečna sprememba plazemskega nivoja prolaktina od osnovne do končne točke v plazmi za skupino, ki je bila zdravljena s FANAPT-om 24 mg / dan, je bilo povečanje za 2,6 ng / ml v primerjavi z zmanjšanjem za 6,3 ng / ml v placebo skupina. V tem preskušanju so pri 26% odraslih, zdravljenih z zdravilom FANAPT, opazili povišano plazemsko raven prolaktina v primerjavi z 12% v skupini s placebom. V kratkotrajnih preskušanjih je bilo zdravilo FANAPT povezano s skromnimi koncentracijami prolaktina v primerjavi z večjimi zvišanjem prolaktina, ki so jih opazili pri nekaterih drugih antipsihotikih. V združeni analizi iz kliničnih študij, vključno z dolgoročnimi preskušanji, je bilo pri 3210 odraslih, zdravljenih z iloperidonom, pri dveh moških (0,1%) poročalo o ginekomastiji. v primerjavi s 0% pri bolnikih, ki so prejemali placebo, in o galaktorreji so poročali pri 8 ženskah (0,2%) v primerjavi s 3 ženskami (0,5%) pri zdravljenju s placebom bolniki.
Regulacija telesne temperature
Motnje telesne sposobnosti, da znižuje telesno temperaturo v jedru, so pripisali antipsihotikom. Pri predpisovanju zdravila FANAPT bolnikom, ki se srečujejo s stanji, ki lahko pripomorejo k zvišanju jedra telesa, svetujemo ustrezno nego. temperatura, npr. naporno treniranje, izpostavljenost izjemni vročini, prejemanje sočasnih zdravil z antiholinergično aktivnostjo ali izpostavljenost dehidracija.
Disfagija
Dismotilnost in aspiracija požiralnika sta povezana z uporabo antipsihotikov. Aspiracijska pljučnica je pogost vzrok obolevnosti in umrljivosti pri starejših bolnikih. Zdravilo FANAPT in druga antipsihotična zdravila je treba uporabljati previdno pri bolnikih, pri katerih obstaja tveganje za aspiracijsko pljučnico.
Samomor
Možnost poskusa samomora je lastna psihotični bolezni, natančen nadzor bolnikov z visokim tveganjem pa mora spremljati zdravljenje z zdravili. Za zmanjšanje tveganja predoziranja je treba napisati recepte za zdravilo FANAPT za najmanjšo količino tablet, skladno z dobrim ravnanjem s pacienti.
Priapizem
V programu FANAPT pred trženjem so poročali o treh primerih priapizma. Poročali so, da zdravila z zaviralnimi učinki alfa-adrenergikov povzročajo priapizem. FANAPT deli to farmakološko aktivnost. Močan priapizem lahko zahteva kirurško posredovanje.
Potencial za kognitivne in motorične okvare
FANAPT, tako kot drugi antipsihotiki, lahko poslabša presojo, mišljenje ali motorične sposobnosti. V kratkotrajnih preskušanjih s placebom so poročali o zaspanosti (vključno s sedacijo) pri 11,9% (104/874) odrasli bolniki, ki so se zdravili z zdravilom FANAPT v odmerkih 10 mg / dan ali več v primerjavi s 5,3% (31/587), ki so jih zdravili placebo. Bolnike je treba opozoriti na delovanje nevarnih strojev, vključno z avtomobili, dokler niso zanesljivo prepričani, da zdravljenje z zdravilom FANAPT nanje ne vpliva negativno.
vrh
Neželeni učinki
Izkušnje s kliničnimi študijami
Ker klinična preskušanja potekajo v zelo različnih pogojih, so v kliničnem preskušanju zdravila opazili stopnjo neželenih učinkov ni mogoče neposredno primerjati s stopnjami v kliničnih preskušanjih drugega zdravila in morda ne odraža hitrosti, opažene v kliničnih preskušanjih vadite. Spodnje informacije so pridobljene iz baze kliničnih preskušanj za FANAPT, sestavljene iz 3229 bolnikov, ki so bili izpostavljeni FANAPT v odmerkih 10 mg na dan ali več, za zdravljenje shizofrenije. Od tega jih je 999 prejelo FANAPT najmanj 6 mesecev, 657 pa jih je bilo izpostavljenih FANAPT vsaj 12 mesecev. Vsi ti bolniki, ki so prejemali zdravilo FANAPT, so sodelovali v kliničnih preskušanjih z več odmerki. Pogoji in trajanje zdravljenja z zdravilom FANAPT so se zelo razlikovali in so bili vključeni (v kategorijah s prekrivanjem), odprto oznako in dvojno slepe faze študij, bolnišnično in ambulantno, študije s fiksnim odmerkom in prilagodljivimi odmerki ter kratkoročne in dolgoročne izpostavljenost.
Podatki, predstavljeni v teh razdelkih, so izhajali iz združenih podatkov s 4 placebo nadzorovanih, 4- ali 6-tedenskih, študije s fiksnim ali prilagodljivim odmerkom pri bolnikih, ki so prejemali FANAPT v dnevnih odmerkih v območju od 10 do 24 mg (n = 874).
Neželeni učinki, ki se pojavljajo pri 2% ali več pri bolnikih, ki se zdravijo s FANAPT, in pogostejši kot pri placebu
Tabela 7 navaja skupne incidente neželenih učinkov, o katerih so spontano poročali v štirih, s placebom nadzorovanih, 4- ali 6-tedenskih, študije s fiksnim ali fleksibilnim odmerkom, v katerih so navedene tiste reakcije pri 2% ali več bolnikov, zdravljenih s FANAPT, pri katerem koli odmerku. skupin in pri katerih je bila incidenca pri bolnikih, zdravljenih s FANAPT-om v kateri koli skupini odmerkov, večja kot incidenca pri bolnikih, zdravljenih z placebo.
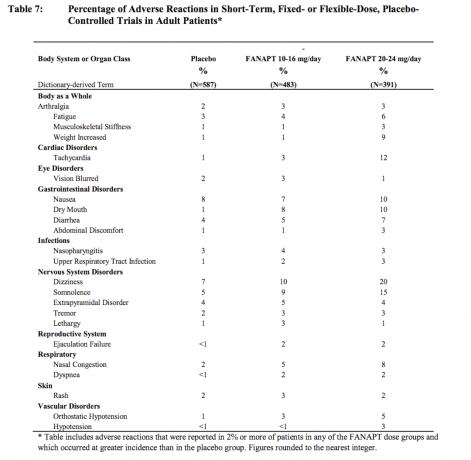
Neželeni učinki v odmerkih v kliničnih preskušanjih
Na podlagi združenih podatkov iz 4 s placebom nadzorovanih, 4- ali 6-tedenskih študij s fiksnim ali prilagodljivim odmerkom neželenih učinkov, ki so se pojavili z več kot 2% incidenca pri bolnikih, ki so se zdravili z zdravilom FANAPT, in pri katerih je bila incidenca pri bolnikih, zdravljenih z zdravilom FANAPT 20-24 mg / dan, dvakrat večja kot incidenca pri bolnikih bolniki, zdravljeni z zdravilom FANAPT 10 -16 mg / dan, so bili: trebušno nelagodje, omotica, hipotenzija, mišično skeletna togost, tahikardija in teža povečala.
Pogosti in z drogami povezani neželeni učinki v kliničnih preskušanjih
Na podlagi združenih podatkov iz štirih s placebom nadzorovanih, 4- ali 6-tedenskih študij s fiksnim ali prilagodljivim odmerkom so se pojavili naslednji neželeni učinki pri ≥5% incidenci pri bolnikih, ki so se zdravili z zdravilom FANAPT in vsaj dvakrat s placebom podgana vsaj za 1 odmerek: omotica, suha usta, utrujenost, nosna kongestija, zaspanost, tahikardija, ortostatska hipotenzija in teža povečala. Omotičnost, tahikardija in povečana teža so bili vsaj dvakrat pogostejši pri 20-24 mg / dan kot pri 10-16 mg / dan.
Ekstrapiramidni simptomi (EPS) v kliničnih preskušanjih
Zbrani podatki iz štirih, s placebom nadzorovanih, 4- ali 6- tedenskih študij s fiksnim ali fleksibilnim odmerkom so zagotovili informacije o EPS. Podatki o neželenih dogodkih, zbrani iz teh preskušanj, so pokazali naslednje stopnje neželenih učinkov, povezanih z EPS, kot so prikazane v tabeli 8.

Neželeni učinki, povezani s prekinitvijo zdravljenja v kliničnih preskušanjih
Na podlagi združenih podatkov iz 4 študij s placebom, 4- ali 6-tedenskimi, fiksnimi ali fleksibilnimi odmerki ni bilo nobenega razlika v pogostnosti prekinitve zdravljenja zaradi neželenih učinkov med zdravljenjem s FANAPT (5%) in s placebom (5%) bolniki. Vrste neželenih učinkov, ki so privedli do prekinitve zdravljenja, so bile podobne pri bolnikih, zdravljenih s FANAPT in pri placebu.
Demografske razlike v neželenih reakcijah v kliničnih preskušanjih
Pregled populacijskih podskupin v 4, s placebom nadzorovanih, 4- ali 6-tedenskih, fiksnih ali študije s prilagodljivim odmerkom niso pokazale nobenih dokazov o razlikah v varnosti glede na starost, spol ali rasa.
Nepravilnosti laboratorijskih testov v kliničnih preskušanjih
Med pogostnostjo prekinitve zdravljenja s FANAPT in placebom ni bilo razlik pri spremembi hematologije, analize urina ali kemije v serumu.
V kratkotrajnih s placebom nadzorovanih preskušanjih (4- do 6 tednov) je bilo 1,0% (13/1342) bolnikov, ki so zdravili iloperidon z hematokrit vsaj enkrat pod podaljšanim normalnim razponom med zdravljenjem po randomizaciji, v primerjavi z 0,3% (2/585) na placebo. Razširjeni normalni razpon za znižani hematokrit je bil opredeljen v vsaki od teh preskušanj kot vrednost 15% pod običajnim območjem za centralizirani laboratorij, ki je bil uporabljen v preskušanju.
Druge reakcije med pred marketinško oceno FANAPT
Sledi seznam izrazov MedDRA, ki odražajo neželene učinke pri bolnikih, ki se zdravijo z zdravilom FANAPT pri več odmerkih ≥ 4 mg / dan med katero koli fazo preskušanja z bazo podatkov 3210, zdravljenih s FANAPT bolniki. Vključene so vse poročane reakcije, razen tistih, ki so že navedene v tabeli 7, ali drugih delov neželenih reakcij (6), ki so obravnavani v Opozorila in previdnostni ukrepi (5), tisti reakcijski izrazi, ki so bili tako splošni, da so neinformativni, o reakcijah, o katerih so poročali pri manj kot treh bolnikih in ki niso bile niti resne niti življenjsko nevarne, reakcije, ki so sicer pogoste kot reakcije v ozadju, in reakcije, za katere je bilo verjetno, da niso droge sorodni.
Reakcije so nadalje razvrščene po organskih sistemih MedDRA in so navedene v zaporedju padajoče pogostosti Opredelitve: pogosti neželeni učinki so tisti, ki se pojavijo pri vsaj 1/100 bolnikov (v tej so le tisti, ki niso navedeni v tabeli 7) kotiranje); redki neželeni učinki so tisti, ki se pojavijo pri 1/100 do 1/1000 bolnikov; redki dogodki so tisti, ki se pojavijo pri manj kot 1/1000 bolnikov.
Krvne in limfne motnje: redko - anemija, anemija s pomanjkanjem železa; Redka levkopenija
Srčne motnje: pogoste - palpitacije; Redke - aritmija, atrioventrikularni blok prve stopnje, srčno popuščanje (vključno s kongestivnim in akutnim)
Bolezni ušesa in labirinta: redko - vrtoglavica, tinitus
Endokrine motnje: redko - hipotiroidizem
Očesne motnje: pogoste - konjunktivitis (vključno z alergičnimi); Redko - suho oko, blefaritis, edem vek, otekanje oči, lentikularne motnosti, katarakta, hiperemija (vključno s konjunktivo)
Bolezni prebavil: redko - gastritis, hipersekrecija sline, inkontinenca fekalija, razjeda v ustih; Redki - aftozni stomatitis, razjeda dvanajstnika, hiatusna kila, hiperhlorhidrija, razjeda ustnic, refluksni ezofagitis, stomatitis
Splošne motnje in administrativni pogoji na mestu: Redko - edemi (splošni, kožni, zaradi srčne bolezni), težave pri hoji, žeja; Redki - hipertermija
Hepatobiliarne motnje: redko - holelitiaza
Preiskave: pogoste: teža se je zmanjšala; Redko - znižal se je hemoglobin, povečalo se je število nevtrofilcev, zmanjšal se hematokrit
Motnje presnove in prehrane: Redko - povečan apetit, dehidracija, hipokalemija, zastajanje tekočine
Bolezni mišično-skeletnega sistema in vezivnega tkiva: pogoste - mialgija, mišični krči; Redki - tortikolis
Bolezni živčnega sistema: redko - parestezija, psihomotorna hiperaktivnost, nemir, amnezija, nistagmus; Redko - sindrom nemirnih nog
Psihiatrične motnje: pogoste - nemir, agresivnost, blodnja; Redko - sovražnost, znižanje libida, paranoja, anorgazmija, konfuzno stanje, manija, katatonija, spremembe razpoloženja, panika napad, obsesivno-kompulzivna motnja, bulimija nervoza, delirij, psihogena polidipsija, motnja nadzora impulza, glavna depresija
Ledvične in sečne motnje: pogoste - urinska inkontinenca; Redko - disurija, pollakiurija, enureza, nefrolitiaza; Redki - zastajanje urina, odpoved ledvic akutna
Motnje reproduktivnega sistema in dojk: pogoste - erektilna disfunkcija; Infrequen - bolečine v testisih, amenoreja, bolečine v prsih; Redki - menstruacija neredna, ginekomastija, menoragija, metroragija, krvavitev v postmenopavzi, prostatitis.
Dihalne, torakalne in mediastinalne motnje: redke - epistaksa, astma, rinoreja, zamašitev sinusa, suhost nosu; Redki - suho grlo, sindrom apneje v spanju, dispneja
Izkušnje po trženju
Med uporabo zdravila FANAPT po odobritvi zdravila FANAPT so bili ugotovljeni naslednji neželeni učinki: retrogradna ejakulacija in preobčutljivostne reakcije (vključno z anafilaksijo; angioedem; tesnost v grlu; oteklina orofaringeusa; otekanje obraza, ustnic, ust in jezika; urtikarija; izpuščaji; in pruritus). Ker so o teh reakcijah poročali prostovoljno iz populacije negotove velikosti, ni mogoče zanesljivo oceniti njihove pogostosti ali vzpostaviti vzročne zveze z izpostavljenostjo drogam.
vrh
Interakcije z zdravili
Glede na primarne učinke zdravila FANAPT na CNS je treba biti previden, če ga jemljemo v kombinaciji z drugimi centralno delujočimi drogami in alkoholom. Zaradi antagonizma receptorjev alfa1-adrenergičnih receptorjev ima FANAPT potencial za povečanje učinka nekaterih antihipertenzivnih zdravil.
Potencial za druge droge, ki vplivajo na FANAPT
Iloperidon ni substrat za encime CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19 ali CYP2E1. To kaže, da interakcija iloperidona z inhibitorji ali induktorji teh encimov ali drugimi dejavniki, kot je kajenje, ni verjetna. Tako CYP3A4 kot CYP2D6 sta odgovorna za presnovo iloperidona. Zaviralci CYP3A4 (npr. Ketokonazol) ali CYP2D6 (npr. Fluoksetin, paroksetin) lahko zavirajo izločanje iloperidona in povzročijo povečano raven v krvi.
Ketokonazol: Sočasna uporaba ketokonazola (200 mg dvakrat na dan 4 dni), močnega zaviralca CYP3A4, s 3 mg enim odmerkom iloperidona na 19 zdravi prostovoljci, stari od 18 do 45 let, so povečali površino pod krivuljo (AUC) iloperidona in njegovih presnovkov P88 in P95 za 57%, 55% in 35%, oz. Pri odmerjanju ketokonazola ali drugih močnih zaviralcev CYP3A4 (npr. Itrakonazola) je treba odmerke iloperidona zmanjšati za približno polovico. Slabih zaviralcev (npr. Eritromicin, grenivkin sok) niso preučevali. Ko se zaviralec CYP3A4 umakne iz kombiniranega zdravljenja, je treba odmerek iloperidona vrniti na prejšnjo raven.
Fluoksetin: Sočasna uporaba fluoksetina (20 mg dvakrat na dan 21 dni), močnega zaviralca CYP2D6, z enim odmerkom 3 mg iloperidona za 23 zdravih prostovoljcev, starih 29–44 let, ki so bili uvrščeni med obsežne metabolizatorje CYP2D6, je povečal AUC iloperidona in njegovega presnovka P88, za približno 2- do 3-krat, in zmanjšal AUC njegovega presnovka P95 za polovica. Odmerke iloperidona moramo zmanjšati za polovico, ko jih dajemo s fluoksetinom. Ko se fluoksetin umakne iz kombiniranega zdravljenja, je treba odmerek iloperidona vrniti na prejšnjo raven. Pričakuje se, da bodo imeli drugi močni zaviralci CYP2D6 podobne učinke in bodo potrebovali ustrezno zmanjšanje odmerka. Ko se zaviralec CYP2D6 umakne iz kombiniranega zdravljenja, se odmerek iloperidona lahko nato poveča na prejšnjo raven.
Paroksetin: Sočasna uporaba paroksetina (20 mg / dan 5-8 dni), močnega zaviralca CYP2D6, z več odmerki iloperidona (8 ali 12 mg dvakrat na dan) bolnikom s shizofrenijo, starimi od 18 do 65 let, kar je povzročilo povečane povprečne najvišje koncentracije v stanju dinamičnega ravnovesja iloperidon in njegov presnovek P88, približno za 1,6 krat, in znižali povprečne najvišje koncentracije metabolita P95 v stanju dinamičnega ravnovesja za polovica. Pri odmerjanju paroksetina je treba odmerke iloperidona zmanjšati za polovico. Ko paroksetin umaknete iz kombiniranega zdravljenja, je treba odmerek iloperidona vrniti na prejšnjo raven. Pričakuje se, da bodo imeli drugi močni zaviralci CYP2D6 podobne učinke in bodo potrebovali ustrezno zmanjšanje odmerka. Ko se zaviralec CYP2D6 umakne iz kombiniranega zdravljenja, se odmerek iloperidona lahko nato poveča na prejšnje ravni.
Paroksetin in ketokonazol: Sočasna uporaba paroksetina (20 mg enkrat na dan 10 dni), zaviralca CYP2D6 in ketokonazola (200 mg dvakrat na dan) z več odmerki iloperidona (8 ali 12 mg dvakrat na dan) bolnikom s shizofrenijo, starimi 18–65 let, je povzročil 1,4 večkratno povečanje koncentracije iloperidona in njegovega presnovka P88 v stanju dinamičnega ravnovesja in 1,4-kratno znižanje P95 v prisotnosti paroksetin. Torej dajanje iloperidona z zaviralci obeh njegovih presnovnih poti ni prispevalo k učinku katerega koli zaviralca, ki se daje sam. Odmerke iloperidona je zato treba zmanjšati za približno polovico, če jih dajemo hkrati z zaviralcem CYP2D6 in CYP3A4.
Zdravilo FANAPT lahko vpliva na druge droge
Študije in vitro na mikrosomih jeter pri ljudeh so pokazale, da iloperidon ne zavira bistveno presnove zdravila, ki se presnavljajo z naslednjimi izocimi citokroma P450: CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9 ali CYP2E1. Poleg tega so raziskave in vitro na mikrosomih jeter pri ljudeh pokazale, da iloperidon ne povzroča encimov lastnosti, posebej za naslednje izocime citokroma P450: CYP1A2, CYP2C8, CYP2C9, CYP2C19, CYP3A4 in CYP3A5
Dekstrometorfan: Študija na zdravih prostovoljcih je pokazala, da se spremembe farmakokinetike dekstrometorfana (odmerek 80 mg) pri odmerku 3 mg sočasno je bil uporabljen iloperidon, kar je povzročilo 17-odstotno povečanje skupne izpostavljenosti in 26-odstotno povečanje najvišjih plazemskih koncentracij C max dekstrometorfan. Zato interakcija med iloperidonom in drugimi substrati CYP2D6 ni verjetna.
Fluoksetin: Enkratni odmerek 3 mg iloperidona ni vplival na farmakokinetiko fluoksetina (20 mg dvakrat na dan).
Midazolam (občutljiv substrat za CYP 3A4): Študija pri bolnikih s shizofrenijo je pokazala manj kot 50% povečanje skupnega midazolama izpostavljenost ravnovesju iloperidona (14 dni peroralnega odmerjanja do 10 mg iloperidona dvakrat na dan) in brez učinka na midazolam C maks. Zato interakcija med iloperidonom in drugimi CYP3A4 substrati malo verjetna.
Zdravila, ki podaljšuje interval QT FANAPT, se ne sme uporabljati z drugimi zdravili, ki podaljšajo interval QT.
vrh
Uporaba v določenih populacijah
Register izpostavljenosti nosečnosti
Obstaja register izpostavljenosti nosečnosti, ki spremlja rezultate nosečnosti pri ženskah, ki so bile med nosečnostjo izpostavljene FANAPT. Za več informacij se obrnite na Nacionalni register nosečnosti za atipične antipsihotike na 1-866-961-2388 ali obiščite http://womensmentalhealth.org/clinical-and -raziskovalni programi / nosečniški register /.
Povzetek tveganja
Novorojenčki, katerih matere so v tretjem trimesečju nosečnosti izpostavljene antipsihotičnim zdravilom, vključno s FANAPT, so po porodu ogrožene za ekstrapiramidne in / ali odtegnitvene simptome. Omejeni razpoložljivi podatki z zdravilom FANAPT pri nosečnicah ne zadostujejo za informacijo o tveganju za večje porodne okvare in splav. Iloperidon ni bil teratogen, če so ga oralno dajali nosečim podganam med organogenezo v odmerkih, ki so bili do 26-krat večji od največjega priporočenega odmerka pri ljudeh 24 mg / dan na osnovi mg / m2. Vendar pa je podaljšalo trajanje nosečnosti in poroda, povečalo še rojstva, zgodnje intrauterine smrti, povečalo pojavnost zamud v razvoju in zmanjšalo preživetje mladičev po porodu. Iloperidon ni bil teratogen, če ga oralno dajemo brejim kuncem med organogenezo v odmerkih do 20-krat s MRHD na osnovi mg / m2. Vendar pa je povečala zgodnje intrauterine smrti in zmanjšala sposobnost ploda ob najvišjem odmerku, ki je bil tudi za materino toksičen odmerek.
Tveganje za večje prirojene okvare in splav za navedeno populacijo ni znano. V splošni populaciji ZDA je ocenjeno tveganje za večje prirojene okvare in splav v klinično priznanih nosečnostih 2-4% oziroma 15-20%.
Klinična vprašanja
Fetalni / neonatalni neželeni učinki
Ekstrapiramidni in / ali odtegnitveni simptomi, vključno z vznemirjenostjo, hipertonijo, hipotonijo, tremorjem, zaspanostjo, respiratorno stisko in Poročali so o motnjah hranjenja pri novorojenčkih, katerih matere so bile v tretjem trimesečju leta 2008 izpostavljene antipsihotikom nosečnost. Ti simptomi so bili v resnosti različni. Nekateri novorojenčki so se okrevali v nekaj urah ali dneh brez posebnega zdravljenja; drugi so zahtevali dolgotrajno hospitalizacijo. Spremljajte novorojenčke za ekstrapiramidne in / ali simptome odtegnitve in ustrezno upravljajte simptome.
Podatki
Podatki o živalih
V raziskavi razvoja zarodkov-ploda so noseče podgane prejemale 4, 16 ali 64 mg / kg / dan (1,6, 6,5 in 26-krat več kot največji priporočeni odmerek za človeka (MRHD) 24 mg / dan na mg / m2) peroralno iloperidona v obdobju organogeneza. Najvišji odmerek je povzročil povečano zgodnjo intrauterino smrt, zmanjšano plodovo težo in dolžino, zmanjšano okostenje okostja ploda in povečano pojavnost manjših skeletnih nepravilnosti ploda in variacije; ta odmerek je povzročil tudi manjšo porabo hrane pri materi in povečanje telesne teže.
V študiji razvoja zarodka-ploda so brejim kuncem v obdobju organogeneze dali 4, 10 ali 25 mg / kg / dan (3, 8 in 20 krat MRHD na osnovi mg / m2) iloperidona. Najvišji odmerek je povzročil povečano zgodnjo intrauterino smrt in zmanjšano sposobnost ploda ob terminu; ta odmerek je povzročil tudi strupenost za mater.
V dodatnih študijah, v katerih so podganom dajali iloperidon v odmerkih, podobnih zgornjim, od začetka pred začetkom sporočanja ali od 17. dan brejosti in nadaljevanje odstavljanja so škodljivi reproduktivni učinki vključevali dolgotrajno nosečnost in porod, povečali stopnja mrtvorojenosti, povečana pojavnost plodnih visceralnih nihanj, zmanjšana teža ploda in mladičev ter manjša poporodna psička preživetje. Učinkov drog na živčno-vedenjski ali reproduktivni razvoj preživelih mladičev ni bilo. Odmerki brez učinka so se gibali od 4 do 12 mg / kg, razen pri povečanju mrtvorojenosti, ki se je zgodil pri najnižjem testiranem odmerku 4 mg / kg, kar je 1,6 krat več kot MRHD na mg / m2. V teh študijah so pri večjih odmerkih opazili strupenost za mater.
Presnov iloperidon P95, ki je glavni krožeči presnovek iloperidona pri ljudeh, vendar ni prisoten v v podganah so bile odmerjene znatne količine podgan v obdobju organogeneze v peroralnih odmerkih 20, 80 ali 200 mg. kg / dan. Niso opazili teratogenih učinkov. Pri vseh odmerkih je prišlo do zapoznele okostnjave okostja. Ni nastala pomembna strupenost za mater. Plazemske ravni P95 (AUC) pri najvišjem testiranem odmerku so bile 2-krat višje kot pri ljudeh, ki so prejemali MRHD iloperidona.
Dojenje
Povzetek tveganja
Podatkov o prisotnosti iloperidona ali njegovih presnovkov v materinem mleku ni učinki iloperidona na dojenega otroka niti vplivi iloperidona na materino mleko proizvodnja. Iloperidon je prisoten v mleku za podgane. Zaradi možnosti resnih neželenih učinkov pri dojenih dojenčkih odsvetujte ženski, da med zdravljenjem z zdravilom FANAPT ne doji.
Podatki Prenos radioaktivnosti v mleko doječih podgan je bil raziskan po enkratnem odmerku [14C] iloperidona v odmerku 5 mg / kg. Koncentracija radioaktivnosti v mleku v 4 urah po odmerjanju je bila približno 10-krat večja od koncentracije v plazmi hkrati. Toda v 24 urah po odmerjanju so koncentracije radioaktivnosti v mleku padle na vrednosti nekoliko nižje kot v plazmi. Presnovni profil v mleku je bil kvalitativno podoben tistemu v plazmi.
Uporaba pri otrocih Varnost in učinkovitost pri otrocih in mladostnikih nista bili ugotovljeni.
Geriatrična uporaba
Klinične študije zdravila FANAPT pri zdravljenju shizofrenije niso vključile zadostnega števila bolniki, stari 65 let in več, da ugotovijo, ali se odzivajo drugače kot mlajši odrasli bolniki. Med 3210 bolniki, zdravljenimi s FANAPT v preskušanjih pred trženjem, je bilo 25 (0,5%) starih ≥65 let in ni bilo bolnikov starih ≥ 75 let.
Pri starejših bolnikih z demenco, povezano s psihozo, zdravljeno s FANAPT, obstaja večje tveganje za smrt v primerjavi s placebom. Zdravilo FANAPT ni odobreno za zdravljenje bolnikov z demenco, povezano s psihozo.
Ledvična okvara
Ker se zdravilo FANAPT močno presnavlja, pri čemer se manj kot 1% zdravila izloči nespremenjeno, le ledvična okvara verjetno ne bo pomembno vplivala na farmakokinetiko zdravila FANAPT. Ledvična okvara (očistek kreatinina <30 ml / min) je imela minimalen učinek na Cmax iloperidona (v enkratnem odmerku 3 mg) in njegovih presnovkov P88 in P95 v katerem koli od izmerjenih 3analitov. AUC0 - ∞ se je pri osebah z okvaro ledvic povečal za 24%, zmanjšal za 6%, pri iloperidonu, P88 in P95 pa za 52%.
Okvara jeter
Pri bolnikih z blago okvaro jeter prilagajanje odmerka FANAPT ni potrebno. Bolniki z zmerno okvaro jeter lahko zahtevajo zmanjšanje odmerka. Zdravila FANAPT ne priporočamo bolnikom s hudo okvaro jeter.
Pri odraslih osebah z blago okvaro jeter niso opazili pomembne razlike v farmakokinetiki iloperidona, P88 ali P95 (skupaj ali nevezano) v primerjavi z zdravimi odraslimi osebami. Pri osebah z zmerno okvaro jeter je bila večja (2-kratna) in bolj spremenljiva prosta izpostavljenost aktivnim presnovkom P88 opazili v primerjavi z zdravimi kontrolami, medtem ko je bila izpostavljenost iloperidonu in P95 na splošno podobna (manj kot 50% sprememb v primerjavi z nadzor). Ker študija pri osebah s hudo jetrno okvaro ni bila izvedena, FANAPT ne priporočamo bolnikom s hudo okvaro jeter.
Status kajenja
Na podlagi raziskav in vitro z uporabo človeških jetrnih encimov FANAPT ni substrat za CYP1A2; kajenje zato ne bi smelo vplivati na farmakokinetiko zdravila FANAPT.
Nosečnost
vrh
Zloraba drog in odvisnost
Nadzorovana snov
FANAPT ni nadzorovana snov.
Zloraba
Zdravila FANAPT sistematično niso preučevali pri živalih ali ljudeh zaradi možnosti zlorabe, strpnosti ali fizične odvisnosti. Medtem ko klinična preskušanja niso pokazala nobene nagnjenosti k vedenju, ki išče zdravilo, ta opažanja niso bila sistematična in niso mogoča na podlagi te izkušnje predvideti, v kolikšni meri se bo zdravilo CNS, FANAPT, enkrat zlorabilo, preusmerilo in / ali zlorabilo tržen. Posledično je treba paciente skrbno oceniti glede zgodovine zlorabe drog in takšni morajo biti natančno opaženo zaradi znakov zlorabe ali zlorabe zdravila FANAPT (npr. razvoj tolerance, povečanje odmerka, iskanje drog vedenje).
vrh
Preveliko odmerjanje
Človeška izkušnja
V predhodnih preskušanjih, ki so vključevala več kot 3210 bolnikov, je prišlo do naključnega ali namernega prevelikega odmerjanja zdravila FANAPT dokumentirano pri 8 bolnikih, od 48 mg do 576 mg, odvzetih naenkrat, in 292 mg, zaužitih v 3 dneh obdobje. Iz teh primerov niso poročali o smrtnih žrtvah. Največje potrjeno enkratno zaužitje zdravila FANAPT je bilo 576 mg; pri tem bolniku niso opazili škodljivih fizičnih učinkov. Naslednja največja potrjena zaužitje zdravila FANAPT je bila 438 mg v 4-dnevnem obdobju; O tem bolniku brez srčnih posledic so poročali o ekstrapiramidnih simptomih in intervalu QTc 507 msec. Ta bolnik je nadaljeval zdravljenje z zdravilom FANAPT dodatnih 11 mesecev.
Na splošno so poročali o znakih in simptomih, ki so posledica pretiravanja z znanimi farmakološkimi učinki (npr. Zaspanost in sedacija, tahikardija in hipotenzija) zdravila FANAPT.
Obvladovanje prevelikega odmerjanja
Za FANAPT ni specifičnega protistrupa. Zato je treba uvesti ustrezne podporne ukrepe. V primeru akutnega prevelikega odmerjanja mora zdravnik vzpostaviti in vzdrževati dihalne poti ter zagotoviti ustrezno oksigenacijo in prezračevanje. Razmisliti je treba o izpiranju želodca (po intubaciji, če je bolnik v nezavesti) in o uporabi aktivnega oglja skupaj z odvajalom. Možnost zaprtja, napadov ali distonična reakcija glave in vratu po prevelikem odmerjanju lahko povzroči nevarnost aspiracije z inducirano bruhanjem. Kardiovaskularno spremljanje se mora začeti takoj in vključevati stalno spremljanje EKG za odkrivanje možnih aritmij. Če se uporablja antiaritmično zdravljenje, disopiramida, prokainamida in kinidina ne smemo uporabljati, saj imajo lahko učinke na podaljšanje QT, ki bi lahko bili dodatki k učinkom zdravila FANAPT. Prav tako je smiselno pričakovati, da bi lastnosti bretilija, ki blokirajo alfa, lahko dodale lastnosti FANAPT, kar bi povzročilo problematično hipotenzijo. Hipotenzijo in prekrvavitev je treba zdraviti z ustreznimi ukrepi, kot so intravenske tekočine ali simpatomimetiki (epinefrina in dopamina se ne sme uporabljati, saj lahko stimulacija beta poslabša hipotenzijo pri nastavitvi alfa, ki jo povzroča FANAPT blokada). V primerih hudih ekstrapiramidnih simptomov je treba dajati antiholinergična zdravila. Pozorni zdravniški nadzor je treba nadaljevati, dokler se bolnik ne okreva.
vrh
Opis
FANAPT je netipičen antipsihotik, ki spada v kemijski razred derivatov piperidinil-benzisoksazola. Njegovo kemijsko ime je 4 '- [3- [4- (6-fluoro-1,2-benzisoksazol-3-il) piperidino] propoksi] -3'-metoksiacetofenon. Njegova molekularna formula je C24H27FN2O4, njegova molekularna teža pa je 426,48. Strukturna formula je:
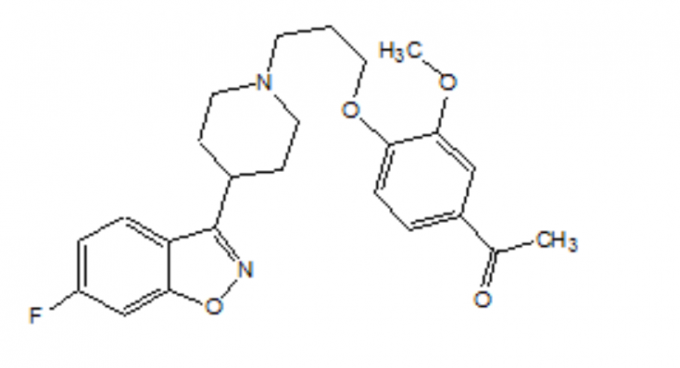
Iloperidon je bel do sivo bel drobno kristalni prah. Praktično je netopen v vodi, zelo slabo topen v 0,1 N HCl in dobro topen v kloroformu, etanolu, metanolu in acetonitrilu.
Tablete FANAPT so namenjene samo peroralnemu dajanju. Vsak krog, brez prevleke
tableta vsebuje 1 mg, 2 mg, 4 mg, 6 mg, 8 mg, 10 mg ali 12 mg iloperidona. Neaktivne sestavine so: laktoza monohidrat, mikrokristalna celuloza, hidroksipropilmetilceluloza, krospovidon, magnezijev stearat, koloidni silicij
dioksid in očiščena voda (odstranjena med predelavo). Tablete so bele, okrogle, ploščate, s poševnimi robovi in označene z logotipom "", vtisnjenim na eni strani in s tabletami "1", "2", "4", "6", "8", "10", ali "12", vtisnjeno na drugi strani.
vrh
Klinična farmakologija
Mehanizem delovanja
Mehanizem delovanja iloperidona pri shizofreniji ni znan. Vendar pa je učinkovitost iloperidona mogoče posredovati s kombinacijo antagonizma dopamina tipa 2 (D2) in serotonina tipa 2 (5-HT2).
Iloperidon tvori aktivni presnovek P88, ki ima profil in vitro vezave na receptorje, podoben matičnemu zdravilu.
Farmakodinamika
Iloperidon deluje kot antagonist z visoko (nM) afinitetno vezavo na serotonin 5-HT2A dopamin D2 in Receptorji D3 in norepinefrinski receptorji NEα1 (vrednosti Ki 5,6, 6,3, 7,1 in 0,36 nM, oz.). Iloperidon ima zmerno afiniteto za receptorje za dopamin D4 in receptorje za serotonin 5-HT6 in 5 -HT7 (vrednosti Ki za 25, 43 in 22, nM ) in nizko afiniteto za receptorje za serotonin 5-HT1A, dopamin D1 in histamin H1 (vrednosti Ki 168, 216 in 437 nM, oz.). Iloperidon nima pomembne afinitete (Ki> 1000 nM) za holinergične muskarinske receptorje. Afiniteta presnovka iloperidona P88 je na splošno enaka ali manjša od matične spojine, medtem ko je samo metabolit P95 kaže afiniteto za 5-HT2A (Ki vrednost 3,91) in receptorje NEα1A, NEα1B, NEα1D in NEα2C (Ki vrednosti 4,7, 2,7, 8,8 in 4,7 nM oz.).
Farmakokinetika
Opaženi povprečni razpolovni čas izločanja iloperidona, P88 in P95 v obsežnih metabolizatorjih CYP2D6 (EM) so 18, 26 in 23 ur, pri slabih metabolizatorjih (PM) pa 33, 37 in 31 ur. Koncentracije v stanju dinamičnega ravnovesja dosežemo v 3 do 4 dneh po odmerjanju. Kopiranje iloperidona je predvidljivo iz farmakokinetike v enem odmerku. Farmakokinetika iloperidona je več kot sorazmerna z odmerkom. Izločanje iloperidona poteka predvsem z jetrno presnovo, ki vključuje 2 P450 izocime, CYP2D6 in CYP3A4.
Absorpcija: Iloperidon se po dajanju tablete dobro absorbira, najvišje plazemske koncentracije v 2 do 4 urah; medtem ko je relativna biološka uporabnost formulacije tablet v primerjavi s peroralno raztopino 96%. Uporaba iloperidona s standardnim obrokom z veliko maščobami ni pomembno vplivala na Cmax ali AUC iloperidona, P88 ali P95, vendar je Tmax zamaknil za 1 uro za iloperidon, 2 uri za P88 in 6 ur za P95. Zdravilo FANAPT se lahko daje ne glede na obroke.
Porazdelitev: Iloperidon ima očitni očistek (očistek / biološka uporabnost) od 47 do 102 L / h, pri čemer je očitna prostornina porazdelitve 1340-2800 L. Pri terapevtskih koncentracijah je nevezani delež iloperidona v plazmi približno 3%, vsakega presnovka (P88 in P95) pa približno 8%.
Presnova in izločanje: Iloperidon se presnavlja predvsem s tremi potmi biotransformacije: redukcija karbonila, hidroksilacija (posredovana s CYP2D6) in O-demetilacija (posredovana s CYP3A4). Prevladujeta presnovka iloperidona, P95 in P88. Presnovek iloperidona P95 predstavlja 47,9% AUC iloperidona in njegovih presnovkov v plazmi v stanju dinamičnega ravnovesja za obsežne metabolizatorje (EM) in 25% za slabe metabolizatorje (PM). Aktivni presnovek P88 predstavlja 19,5% in 34,0% celotne izpostavljenosti plazmi v EM in PM oz.
Približno 7% -10% belcev in 3% -8% temnopoltih / Afroameričanov nima zmogljivosti za presnovo CYP2D6 substrati in jih uvrščamo med slabe metabolizatorje (PM), preostali pa so vmesni, ekstenzivni ali ultrarapid metabolizatorji. Sočasna uporaba zdravila FANAPT z znanimi močnimi zaviralci CYP2D6, kot je fluoksetin, povzroči 2,3-krat povečanje izpostavljenosti iloperidonu v plazmi, zato mora biti polovica odmerka FANAPT upravlja.
Prav tako imajo PM-ji CYP2D6 večjo izpostavljenost iloperidonu v primerjavi z EM-ji in PM-ji naj bi odmerek zmanjšali za polovico. Na voljo so laboratorijski testi za prepoznavanje PM v CYP2D6.
Glavnina radioaktivnih snovi je bila odkrita z urinom (povprečno 58,2% in 45,1% v EM in PM), z blatom pa 19,9% (EM) do 22,1% (PM) odmerjene radioaktivnosti.
Interakcija transporterjev: Iloperidon in P88 nista substrata P-gp in iloperidon je šibek zaviralec P-gp.
vrh
Neklinična toksikologija
Kancerogeneza, mutageneza, oslabitev plodnosti
Karcinogeneza: Vseživljenjske študije kancerogenosti so bile izvedene na miših CD-1 in podganah Sprague Dawley. Iloperidon so dajali mišicam CD-1 peroralno v odmerkih 2,5, 5,0 in 10 mg / kg / dan ter 4, 8 in 16 mg / kg / dan za Podgane Sprague Dawley (0,5, 1,0 in 2,0 krat ter 1,6, 3,2 in 6,5-krat, MRHD 24 mg / dan na mg / m2 osnova). Povečal se je pojavnost malignih tumorjev mlečnih žlez pri samicah miši, ki so bile zdravljene samo z najnižjim odmerkom (2,5 mg / kg / dan). Pri podganah ni bilo povezanih z zdravljenjem povečanj neoplazije.
Kancerogeni potencial presnovka iloperidona P95, ki je glavni krožeči presnovek iloperidona pri ljudeh, vendar v mišicah oz. podgane, so v raziskavi kancerogenosti v življenju pri podganah Wistar ocenili pri peroralnih odmerkih 25, 75 in 200 mg / kg / dan pri samcih ter 50, 150 in 250 (zmanjšanih od 400) mg / kg / dan v samice. Z drogami povezane neoplastične spremembe so se pojavile pri moških, v hipofizi (pars distalis adenoma) pri vseh odmerkih in v visokem odmerku v trebušni slinavki (otočni celični adenom). Plazemske ravni P95 (AUC) pri moških v testiranih odmerkih (25, 75 in 200 mg / kg / dan) so bile približno 0,4, 3 in 23-krat večje od izpostavljenosti človeka P95 pri MRHD iloperidona.
Mutageneza: Iloperidon je bil negativen v Amesovem testu in v in vivo testih na mišičnem mozgu na mišji in jetrni mikroklini. Kromosomske aberacije inducirane z iloperidonom in vitro v celicah kitajskega hrčka (CHO) v koncentracijah, ki so prav tako povzročile določeno citotoksičnost.
Preskus iloperidon P95 je bil negativen pri Amesovem testu, preskusu aberacije kromosomske aberacije V79 in in vivo mikronukleusnem testu mišičnega mozga in vivo.
Oslabitev plodnosti: V študiji, v kateri so zdravili podgane in samce, so iloperidon zmanjšali plodnost pri 12 in 36 mg / kg. Odmerek brez učinka je bil 4 mg / kg, kar je 1,6 krat MRHD za 24 mg / dan na osnovi mg / m2.
vrh
Klinične študije
Učinkovitost zdravila FANAPT pri zdravljenju shizofrenije je podprla 2 placebo in aktivno kontrolirano kratkotrajno (4- in 6-tedensko) preskušanje in eno dolgoročno placebo-kontrolirano randomizirano sojenje za umik. V vsa preskušanja so bili vključeni bolniki, ki so za shizofrenijo izpolnjevali merila DSM-III / IV.
V teh študijah so bili uporabljeni trije instrumenti za oceno psihiatričnih znakov in simptomov. Pozitivna in negativna lestvica sindroma (PANSS) in kratka lestvica psihiatričnega ocenjevanja (BPRS) sta zaloga več postavk.
splošne psihopatologije, ki se običajno uporablja za oceno učinkov zdravljenja s shizofrenijo. Ocena klinične globalne impresije (CGI) odraža vtis usposobljenega opazovalca, ki je v celoti seznanjen s manifestacijami shizofrenije, o celotnem kliničnem stanju pacienta.
6-tedensko, s placebom nadzorovano preskušanje (n = 706) je vključevalo 2 prožni odmerki FANAPT-a (12-16 mg / dan ali 20-24 mg / dan) v primerjavi s placebom in aktivnim nadzorom (risperidon). Za skupino 12-16 mg / dan je bila shema titracije FANAPT 1 mg dvakrat na dan 1. in 2. dan, 2 mg dvakrat na dan 3. in 4. dan, 4 mg dvakrat na dan 5. in 6. dan ter 6 mg dvakrat dnevno vsak dan na 7. dan. Za skupino 20-24 mg / dan je bila shema titracije FANAPT 1 mg dvakrat na dan 1. dne 2 mg dvakrat na dan 2. dan, 4 mg dvakrat na dan 3. dan, 6 mg dvakrat na dan 4. in 5. dan, 8. dan dvakrat na dan, 6. dan pa 8 mg dvakrat dnevno. Primarna končna točka je bila sprememba glede na izhodišče glede na skupni rezultat BPRS na koncu zdravljenja (42. dan). Tako 12-16 mg / dan kot 20-24 mg / dan odmerka zdravila FANAPT sta bila boljša od placeba glede na skupni rezultat BPRS. Zdi se, da je bilo v prvem preskušanju aktivno antipsihotično zdravilo v tem preskusu boljše kot FANAPT tedne, ugotovitev, ki se lahko deloma razloži s hitrejšim titracijo, ki je bilo mogoče za to droga. Pri bolnikih v tej študiji, ki so bili na zdravljenju vsaj 2 tedna, se je zdelo, da je imel iloperidon učinkovitost kot primerljivo pri aktivni kontroli.
4-tedensko, s placebom nadzorovano preskušanje (n = 604) je vključevalo en fiksni odmerek FANAPT (24 mg / dan) v primerjavi s placebom in aktivni nadzor (ziprasidon). Urnik titracije za to študijo je bil podoben kot v 6-tedenski študiji. Ta študija je vključevala titracijo zdravila FANAPT, ki se je začela na 1 mg dvakrat na dan na 1. dan in povečala na 2, 4, 6, 8, 10 in 12 mg dvakrat na dan 2., 3., 4., 5., 6. in 7. dan. Primarna končna točka je bila sprememba glede na izhodišče glede na skupni rezultat PANSS na koncu zdravljenja (28. dan). 24-miligramski odmerek FANAPT na dan je bil v skupni oceni PANSS večji od placeba. Zdi se, da ima zdravilo FANAPT podobno učinkovitost kot aktivno kontrolno zdravilo, ki je prav tako zahtevalo počasno titracijo do ciljnega odmerka.
V dolgoročnejšem preskušanju so klinično stabilne odrasle ambulante (n = 303), ki izpolnjujejo merila DSM-IV za shizofrenijo, ki je ostala stabilna po 12 tednih odprto zdravljenje z fleksibilnimi odmerki zdravila FANAPT (8 mg / dan - 24 mg / dan, ki ga dajemo kot odmerke dvakrat na dan) smo randomizirali na placebo ali nadaljevali z njihov trenutni odmerek FANAPT (8 mg / dan - 24 mg / dan, ki ga dajemo kot dvakrat na dan) za opazovanje možnih ponovitev med dvojno slepim relapsom faza preprečevanja. Stabilizacijo med odprto fazo je bilo opredeljeno tako, da je bila na določenem odmerku zdravila FANAPT, ki je bil v 4 tednih pred randomizacijo nespremenjen zaradi učinkovitosti, z oceno CGI-resnosti ≤4 in skupno skupno oceno PANSS ≤70, oceno ≤4 na vsaki od naslednjih posameznih postavk PANSS (P1-blodnje, P2-konceptualna neorganizacija, P3 halucinacijsko vedenje, sumnjičavost / preganjanje P6, sovražnost P7 ali nesodelovanje z G8) in brez hospitalizacije ali povečanja ravni oskrbe za zdravljenje poslabšanja. Ponovni ali bližajoči se recidivi med dvojno slepo fazo preprečevanja ponovitev so bili opredeljeni kot kateri koli od naslednje: hospitalizacija zaradi poslabšanja shizofrenije, povečanje (poslabšanje) skupne ocene PANSS ≥30%, CGI-
Rezultat izboljšanja ≥ 6, je imel bolnik samomorilno, ubojno ali agresivno vedenje ali potrebo po kakšnih drugih antipsihotičnih zdravilih.

Na podlagi vmesne analize je neodvisni odbor za spremljanje podatkov sklenil, da je treba študijo prekiniti zaradi dokazov o učinkovitosti. Na podlagi rezultatov vmesne analize, ki jih je potrdil končni nabor podatkov, so bolniki zdravili Zdravilo FANAPT je imelo statistično pomemben daljši čas ponovitve ali bližajočega se recidiva kot pri bolnikih, ki so ga prejeli placebo. Slika 1 prikazuje ocenjeni kumulativni delež bolnikov z relapsom ali bližajočim se relapsom na podlagi končnega nabora podatkov.
vrh
Kako dobava / skladiščenje in ravnanje
Tablete FANAPT so bele, okrogle in označene z logotipom, na eni strani z vtisnjenim logotipom in s tableto "1", "2", "4", "6", "8", "10" ali "12". strani. Tablete so na voljo v naslednjih jakostih in konfiguracijah paketov:
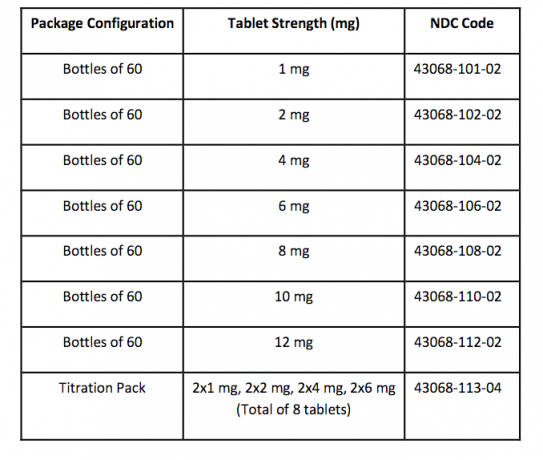
Skladiščenje
Shranjujte tablete FANAPT pri nadzorovani sobni temperaturi, 25 ° C (77 ° F); izleti dovoljeni na 15 ° do 30 ° C (59 ° do 86 ° F) [Glej USP nadzorovana temperatura prostora]. FANAPT tablete zaščitite pred izpostavljenostjo svetlobi in vlagi.
INFORMACIJE O BOLNIČKEM SVETOVANJU
Zdravnikom svetujemo, da se z bolniki, ki jim predpišejo zdravilo FANAPT, pogovorijo o naslednjih težavah:
Podaljševanje intervala QT
Bolnike je treba opozoriti, naj se nemudoma posvetujejo s svojim zdravnikom, če se počutijo omedlevice, izgubijo zavest ali trpijo srce. Bolnikom je treba svetovati, naj zdravila FANAPT ne jemljejo skupaj z drugimi zdravili, ki povzročajo podaljšanje intervala QT. Bolnike je treba opozoriti, naj zdravnike obvestijo, da jemljejo zdravilo FANAPT, preden jemljejo novo zdravilo.
Nevroleptični maligni sindrom
Bolnikom in skrbnikom je treba svetovati, da se včasih napoti potencialno smrtni kompleks simptomov kot so poročali o NMS v povezavi z dajanjem antipsihotikov, vključno s FANAPT. Znaki in simptomi NMS vključujejo hiperpireksijo, togost mišic, spremenjen duševni status in dokaze o samostojnosti
nestabilnost (nepravilen pulz ali krvni tlak, tahikardija, diaforeza in srčna disitmija).
Presnovne spremembe
Bolniki se morajo zavedati simptomov hiperglikemije (visokega krvnega sladkorja) in diabetesa mellitusa. Bolniki z diagnozo sladkorne bolezni, tisti z dejavniki tveganja za nastanek sladkorne bolezni ali pa tisti, ki jih razvijejo simptomi med zdravljenjem bi morali spremljati koncentracijo glukoze v krvi na začetku in občasno zdravljenje. Bolnikom je treba svetovati, da je med zdravljenjem z zdravilom FANAPT prišlo do povečanja telesne mase. Priporočljivo je klinično spremljanje teže.
Ortostatska hipotenzija
Bolnike je treba opozoriti na tveganje za ortostatsko hipotenzijo, zlasti v času začetka zdravljenja, ponovnega uvajanja zdravljenja ali povečanja odmerka.
Motnje v kognitivnih in motoričnih zmogljivostih
Ker lahko zdravilo FANAPT poslabša presojo, razmišljanje ali motorične spretnosti, je treba bolnike opozoriti delovanje nevarnih strojev, vključno z avtomobili, dokler niso povsem prepričani, da terapija s FANAPT ne vpliva nanje negativno.
Nosečnost
Bolnikom svetujte, da lahko uporaba zdravila Fanapt v tretjem trimesečju povzroči ekstrapiramidne in / ali odtegnitvene simptome pri novorojenčku. Pacientom svetujte, naj obvestijo svojega zdravnika z znano ali sumljivo nosečnostjo.
Register nosečnosti
Pacientom svetujte, da obstaja register izpostavljenosti nosečnosti, ki spremlja rezultate nosečnosti pri ženskah, ki so bile med nosečnostjo izpostavljene FANAPT
Dojenje
Ženskam svetujte, naj med zdravljenjem z zdravilom FANAPT ne dojijo.
Sočasno zdravljenje z zdravili
Bolnike je treba opozoriti, naj obvestijo svoje zdravnike, če jemljejo ali načrtujejo jemanje katerega koli zdravila na recept ali več kot na recept, saj lahko pride do interakcij.
Alkohol
Bolnike je treba opozoriti, naj med jemanjem zdravila FANAPT izogibajo alkoholu.
Izpostavljenost toploti in dehidracija
Bolnike je treba svetovati glede ustrezne nege pri preprečevanju pregrevanja in dehidracije.
Distributer:
Vanda Pharmaceuticals Inc.
Washington, D.C. 20037 ZDA
Vanda in Fanapt® sta registrirani blagovni znamki Vanda Pharmaceuticals Inc. v ZDA in drugih državah.
nazaj na vrh
Priročnik za predpisovanje zdravila Fanapt (Iloperidon) (PDF)
Informacije v tej monografiji ne zajemajo vseh možnih načinov uporabe, navodil, previdnostnih ukrepov, interakcij z zdravili ali škodljivih učinkov. Te informacije so posplošene in niso mišljene kot poseben zdravniški nasvet. Če imate vprašanja o zdravilih, ki jih jemljete ali bi želeli več informacij, se posvetujte s svojim zdravnikom, farmacevtom ali medicinsko sestro.
nazadnje posodobljeno 07/13
nazaj k: Domača stran Psihiatrična zdravila



